MINIGUÍA CLÍNICA
Cataratas
Detección, clasificación y derivación para el optometrista
Ficha rápida
El oftalmólogo es quien diagnostica y trata las cataratas. El optometrista debe tener conocimientos sobre las cataratas para derivar los casos sospechosos.
Factores de riesgo
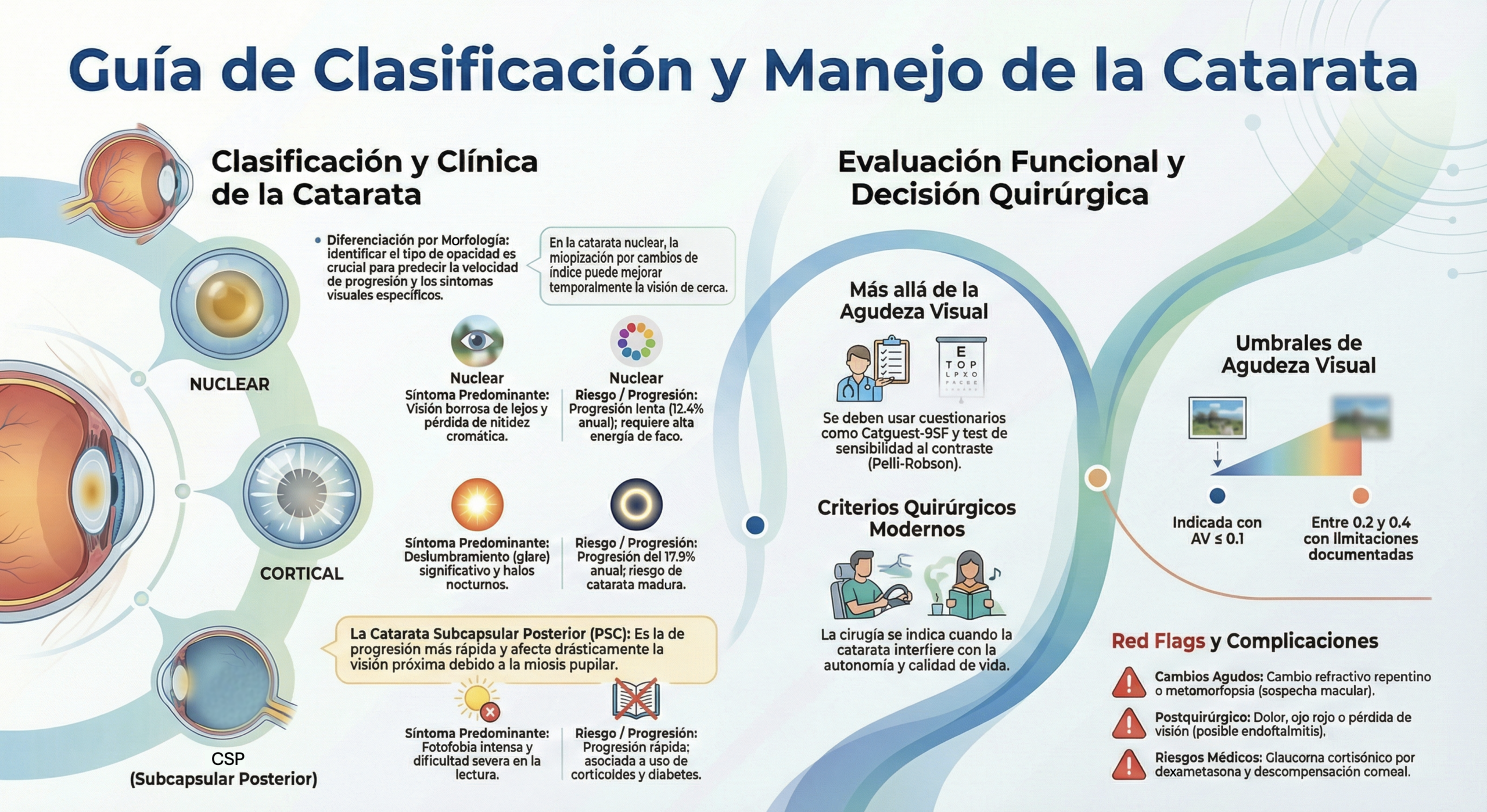
La catarata senil es multifactorial. Aunque la edad es el principal factor, existen factores modificables que el optometrista puede identificar y sobre los que puede educar al paciente.
Factores no modificables
Factores modificables
Catarata precoz (<50 años) o subcapsular posterior en joven: pensar siempre en corticoides (sistémicos, inhalados o tópicos), diabetes, trauma o uveítis crónica. No es “normal”: requiere investigación etiológica.
Clasificación clínica
La clasificación por tipo morfológico y gravedad es esencial para documentar, comunicar con el oftalmólogo y planificar la derivación. El sistema LOCS III (Lens Opacities Classification System III) es el estándar de referencia [7].
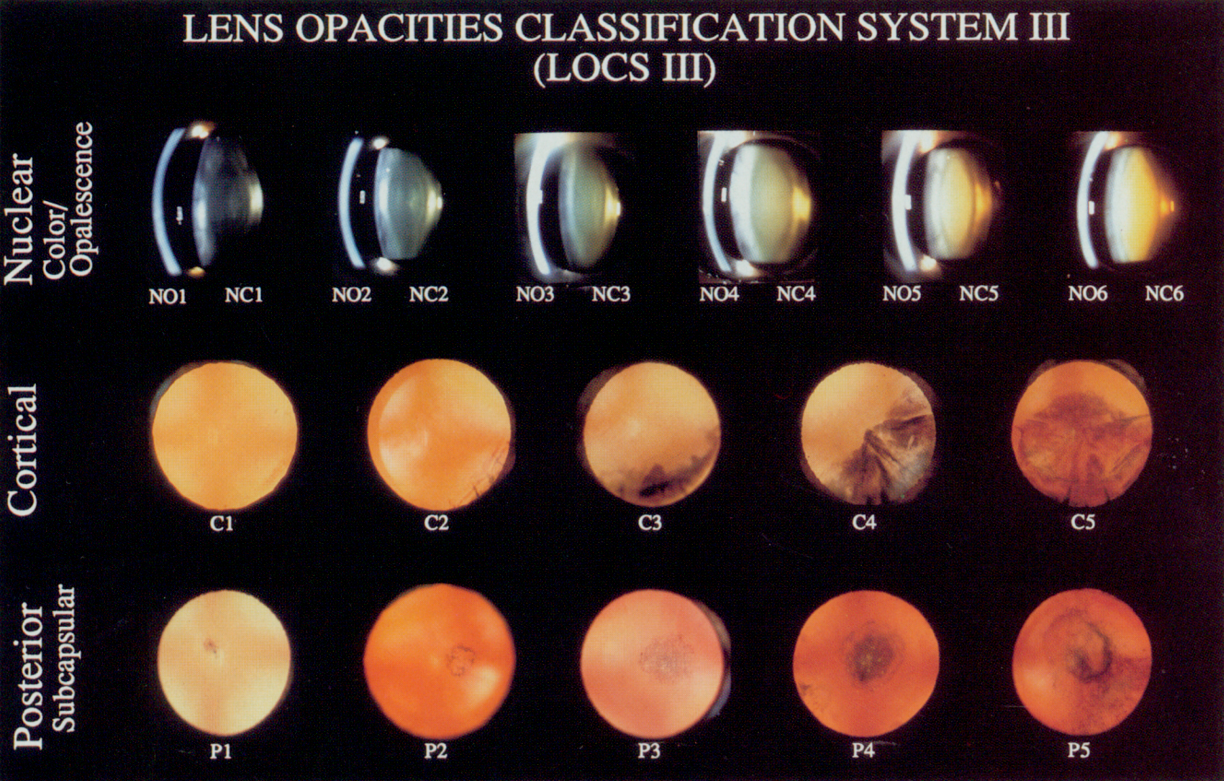
Sistema de clasificación opacidad lenticular LOCS III
Tipos morfológicos
Graduación de severidad (escala clínica simplificada)
La “segunda visión” (second sight) es común en catarata nuclear: el paciente nota que lee mejor sin gafas de cerca porque la esclerosis nuclear induce un shift (cambio) miópico de -1.00 a -3.00 D. Si el paciente dice “mi visión de cerca ha mejorado”, pensar en posible catarata nuclear.
Protocolo de evaluación optométrica
El optometrista es a menudo el primer profesional que detecta la catarata. Una evaluación sistemática permite documentar el tipo y gravedad, descartar comorbilidades oculares, y derivar con información de calidad.
Anamnesis dirigida
- Síntomas visuales: visión borrosa progresiva, glare/deslumbramiento, diplopía monocular, cambios frecuentes de graduación, dificultad en conducción nocturna, alteración percepción de colores (amarillamiento)
- Impacto funcional: conducción, lectura, trabajo, actividades cotidianas, caídas. El impacto funcional, no solo la AV, determina el momento de la derivación quirúrgica
- Medicación: corticoides (orales, inhalados, tópicos oculares), tamoxifeno, amiodarona, clorpromazina, alopurinol
- Comorbilidades: diabetes, uveítis, glaucoma, distrofia miotónica, síndrome de Down, dermatitis atópica
- Historial ocular: trauma, cirugía previa (vitrectomía, glaucoma), inyecciones intravítreas
Evaluación clínica
Agudeza visual y refracción
- AVMC lejos y cerca. Refracción actualizada: descartar que la pérdida visual sea refractiva corregible
- Cambio miópico nuevo en paciente >50 años: sospechar esclerosis nuclear
- Agudeza con agujero estenopeico: si mejora significativamente, existe componente refractivo; si no mejora, la opacidad del medio es la causa principal
Biomicroscopía (lámpara de hendidura)
- Herramienta principal de detección y clasificación
- Evaluación sistemática: cápsula anterior, corteza anterior, núcleo (color y opalescencia), corteza posterior, cápsula posterior
- Retroiluminación: imprescindible para detectar opacidades corticales y PSC
- Documentar tipo (N/C/PSC/mixta) y grado aproximado (1+ a 4+)
Reflejo rojo (oftalmoscopía directa / retinoscopía)
- Un reflejo rojo reducido, irregular o ausente indica opacidad significativa del cristalino
- La retinoscopía muestra sombras “en tijera” o irregularidades del reflejo con cataratas corticales
Fondo de ojo
- Si la catarata impide ver el fondo: documentar y comunicar al oftalmólogo
Tonometría
- Documentar y derivar si hay elevación o asimetría de la presión intraocular
Pruebas complementarias según disponibilidad
- OCT macular: descartar EMD, DMAE, membrana epirretiniana. Pronóstico visual postcirugía
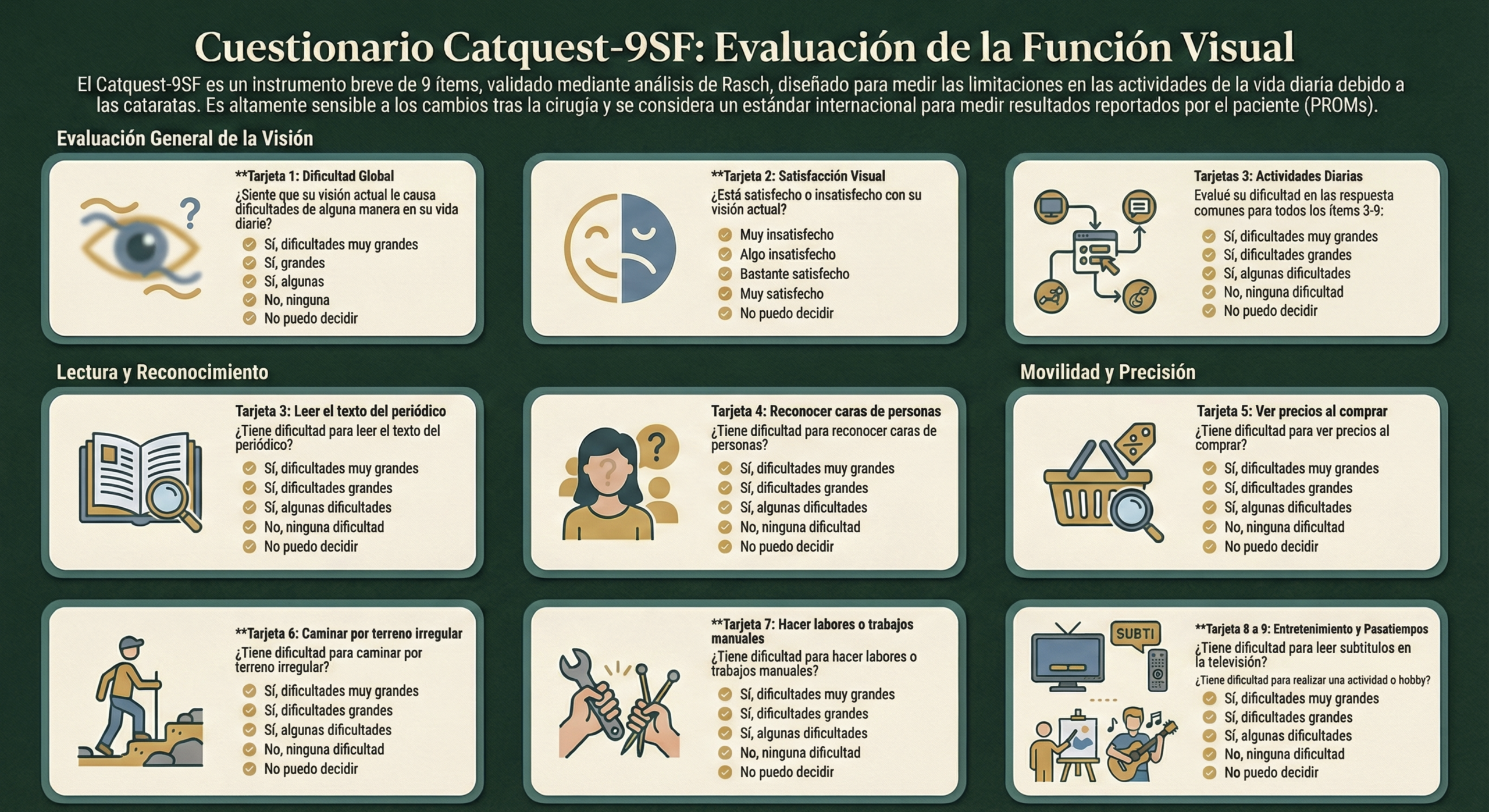
- Sensibilidad al contraste y test de deslumbramiento (glare): objetivan el impacto funcional cuando la AV parece “aceptable” pero el paciente refiere síntomas
La AV no es el único criterio de derivación. Un paciente con AV de 0.7 pero glare severo que le impide conducir de noche tiene indicación de evaluación quirúrgica. El test de deslumbramiento y la evaluación funcional son herramientas clínicas infrautilizadas en optometría.
Manejo y opciones quirúrgicas
No existe tratamiento médico eficaz para revertir la catarata. La cirugía es el único tratamiento definitivo. El optometrista maneja las cataratas incipientes y deriva cuando existe indicación.
Manejo conservador (cataratas leves-moderadas)
- Actualización de la graduación: el paciente puede beneficiarse de una prescripción actualizada durante meses o años antes de necesitar cirugía
- Lentes con filtro UV y antirreflectante: reducen glare y protegen contra progresión UV-dependiente
- Iluminación adecuada: recomendar luz directa sobre el material de lectura, evitar fuentes de luz que generen deslumbramiento
- Educación preventiva: protección solar, cese tabáquico, control de diabetes, nutrición rica en antioxidantes
- Seguimiento: cada 6-12 meses según grado. Documentar AV, tipo/grado de catarata, y cambios entre visitas
Cirugía de cataratas (lo que el optometrista debe conocer)
Lentes intraoculares (LIO)
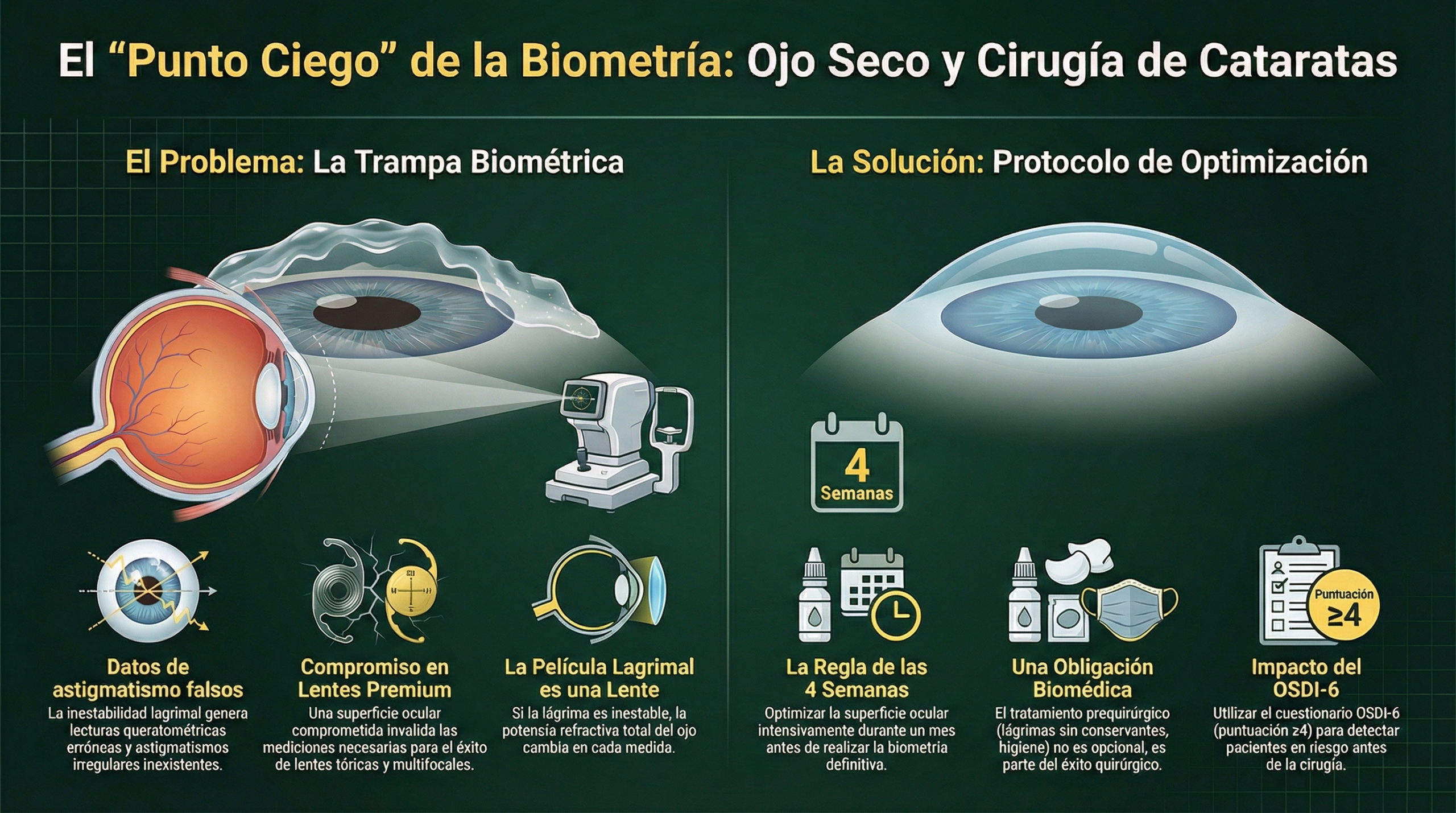
El optometrista informado sobre tipos de LIO puede orientar al paciente ANTES de la consulta quirúrgica, gestionando expectativas y facilitando la decisión. Recuerda: optimizar la superficie ocular 4 semanas antes de la biometría es obligatorio (véase Miniguía Ojo Seco). Una superficie comprometida invalida las mediciones y puede llevar a errores refractivos postquirúrgicos.
Señales de alarma y criterios de derivación
Derivación urgente (24-48 horas)
- Catarata intumescente con cámara anterior estrecha y/o PIO elevada (riesgo de glaucoma facolítico/facomorfótico)
- Pérdida visual súbita en ojo con catarata conocida (descartar patología retiniana aguda no visible por la opacidad)
- Leucocoria en adulto o niño (descartar retinoblastoma en niños, catarata madura en adultos)
- Uveítis activa con catarata complicada progresiva
Derivación programada (criterios de indicación quirúrgica)
- AV ≤0.5 con impacto funcional (o inferior al umbral requerido para conducción: 0.5 binocular en España)
- Glare o pérdida de sensibilidad al contraste que limita actividades cotidianas, aunque la AV sea ≥0.5
- Catarata que impide el diagnóstico o seguimiento de patología retiniana (DMAE, RD, glaucoma): indicación médica de cirugía
- Anisometropía inducida por la catarata que impide corrección óptica satisfactoria
- Paciente que desea cirugía refractiva combinada (catarata + presbicia/astigmatismo): informar y derivar con evaluación completa
Seguimiento optométrico activo (no derivar aún)
- Catarata grado 1+: seguimiento anual. Actualizar graduación si necesario
- Catarata grado 2+: seguimiento cada 6 meses. Documentar progresión
- Catarata leve sin impacto funcional: educación sobre factores protectores (UV, tabaco, nutrición)
- Post-cirugía estabilizada: comanejo con oftalmólogo. AV, refracción final (3-4 semanas post), PIO, estado de la cápsula posterior (OCP a los 6-12 meses)
Consideraciones especiales
Catarata y ojo seco: el círculo vicioso
La cirugía de cataratas puede inducir o empeorar el ojo seco (interrupción nerviosa corneal, exposición a luz del microscopio, conservantes tópicos postquirúrgicos). A su vez, el ojo seco preoperatorio invalida la biometría y topografía. Protocolo: optimizar superficie ocular 4 semanas ANTES de la biometría. Postcirugía: lubricación intensiva 3-6 meses. Véase Miniguía Ojo Seco.
Catarata y diabetes
Los diabéticos desarrollan cataratas antes y más frecuentemente. La cirugía puede empeorar el edema macular diabético preexistente. En pacientes con RD, estabilizar el EMD antes de operar es crítico. Control de HbA1c perioperatorio: objetivo <8% para minimizar complicaciones. Véase Miniguía EMD.
Catarata y glaucoma
Coexistencia frecuente. La facoemulsificación per se puede reducir la PIO 1-4 mmHg (efecto hipertensivo del cristalino eliminado). En glaucoma avanzado, cirugía combinada (faco + MIGS) es una opción creciente. PIO elevada con catarata intumescente: urgencia quirúrgica. Véase Miniguía Glaucoma.
Opacificación de la cápsula posterior (OCP)
La OCP es la complicación postquirúrgica más frecuente (20-50% a los 2-5 años). El paciente refiere pérdida visual progresiva similar a la catarata original. Tratamiento: capsulotomía YAG (procedimiento láser ambulatorio, rápido, definitivo). El optometrista detecta la OCP en lámpara de hendidura y deriva para YAG.
Comanejo postquirúrgico
El optometrista puede participar en el seguimiento postquirúrgico: evaluación de AV a las 24-48h, control de PIO y estado inflamatorio a la semana, refracción definitiva a las 3-4 semanas, detección de OCP en el seguimiento a largo plazo. La colaboración optometrista-oftalmólogo en el circuito de catarata libera consultas hospitalarias y mejora el acceso.
Checklist para la práctica clínica
- Refracción actualizada antes de atribuir la pérdida visual a la catarata. Test de agujero estenopeico
- Biomicroscopía: documentar tipo (N/C/PSC/mixta) y grado (1+ a 4+)
- Fondo de ojo: si la catarata impide ver el fondo, documentar y comunicar al oftalmólogo
- Tonometría: documentar y derivar si hay elevación o asimetría de la presión intraocular
- Evaluar impacto funcional (no solo AV): glare, conducción, lectura, trabajo, caídas
- OCT macular si disponible: descartar EMD, DMAE, MER (pronóstico visual postcirugía)
- Superficie ocular: evaluar ojo seco antes de derivar a cirugía (biometría fiable requiere superficie sana)
- Catarata precoz (<50 años) o PSC en joven: investigar causa (corticoides, DM, trauma, uveítis)
- Informe de derivación: AV, tipo/grado catarata, PIO, hallazgos de fondo, comorbilidades, medicación
- URGENTE si: catarata intumescente + PIO elevada, pérdida visual súbita, leucocoria, uveítis activa complicada
Este documento es informativo y no sustituye ni a una consulta médica ni optométrica. El diagnóstico definitivo y el plan de tratamiento deben ser efectuados, según el caso, por su oftalmólogo o por su optometrista.
Referencias bibliográficas
- Hashemi H, Pakzad R, et al. (2020). Global and regional prevalence of age-related cataract: a comprehensive systematic review and meta-analysis. Eye, 34, 1357-1370.
- GBD 2021 Cataract Collaborators (2025). Global prevalence and years lived with disability (YLDs) of cataract in 204 countries and territories: findings from the GBD Study 2021. Eye (publicado marzo 2025).
- Hashemi H, Fayaz F, et al. (2025). Global prevalence of cataract surgery. Curr Opin Ophthalmol, 36(1), 10-17.
- World Council of Optometry (2025). Standard of Care for Presbyopia and the Aging Eye. Resoluciones basadas en evidencia.
- Prokofyeva E, Wegener A, Zrenner E. (2013). Cataract prevalence and prevention in Europe: a literature review. Acta Ophthalmol, 91(5), 395-405.
- Liu YC, Wilkins M, Kim T, et al. (2017). Cataracts. Lancet, 390(10094), 600-612.
- Chylack LT Jr, Wolfe JK, Singer DM, et al. (1993). The Lens Opacities Classification System III. Arch Ophthalmol, 111(6), 831-836.
- Stern B, Findl O, et al. (2025). Presbyopia Correction in Lens Replacement Surgery: A Review. Clin Exp Ophthalmol (publicado abril 2025).