MINIGUÍA CLÍNICA
Degeneración Macular Asociada a la Edad (DMAE)
Ficha rápida
El oftalmólogo es quien diagnostica y trata la DMAE. El optometrista debe tener conocimientos sobre la DMAE para derivar los casos sospechosos.

Factores de riesgo
La identificación sistemática de factores de riesgo permite estratificar pacientes, personalizar la frecuencia de seguimiento y orientar la educación sobre modificaciones del estilo de vida con impacto real en la progresión.
Factores no modificables
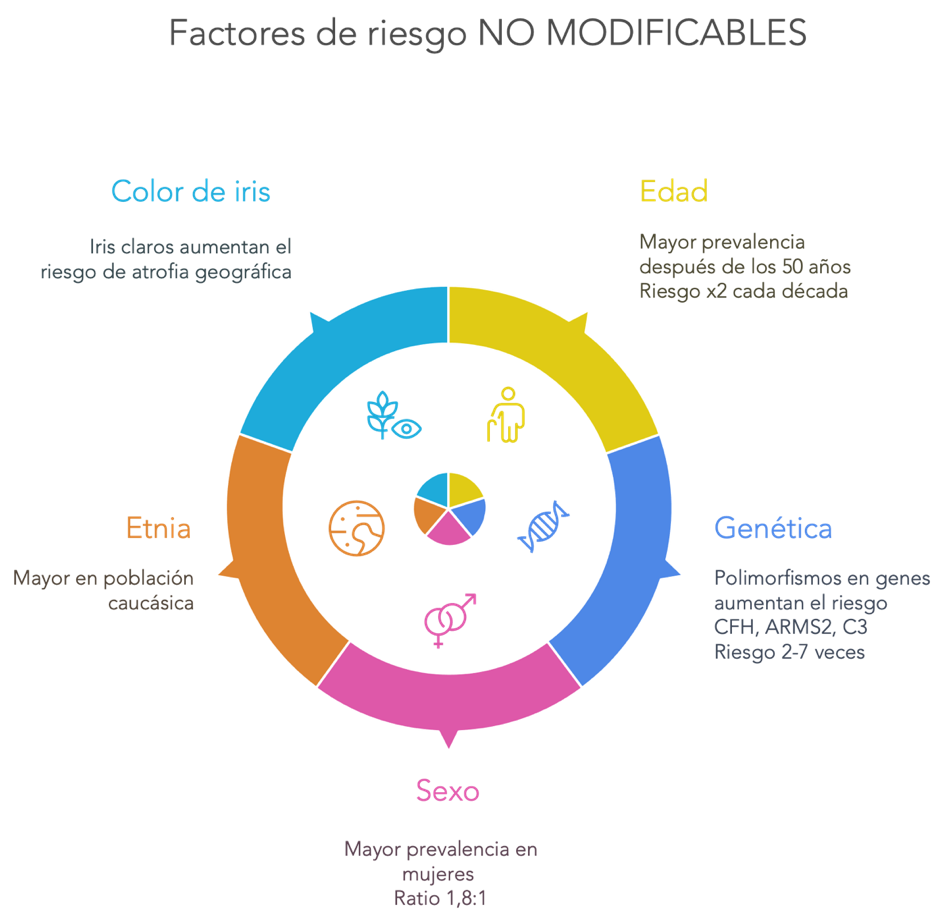
Factores modificables
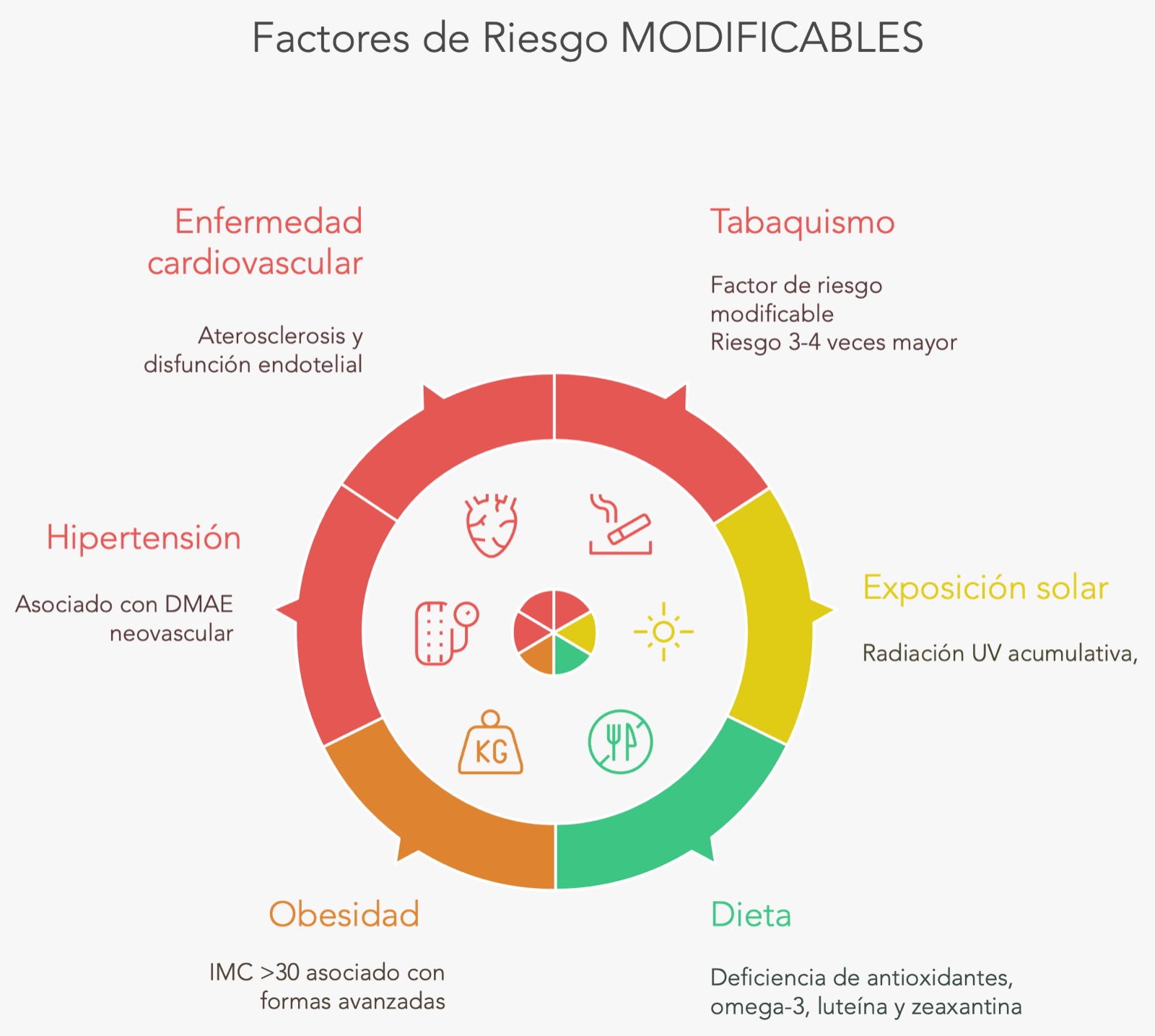
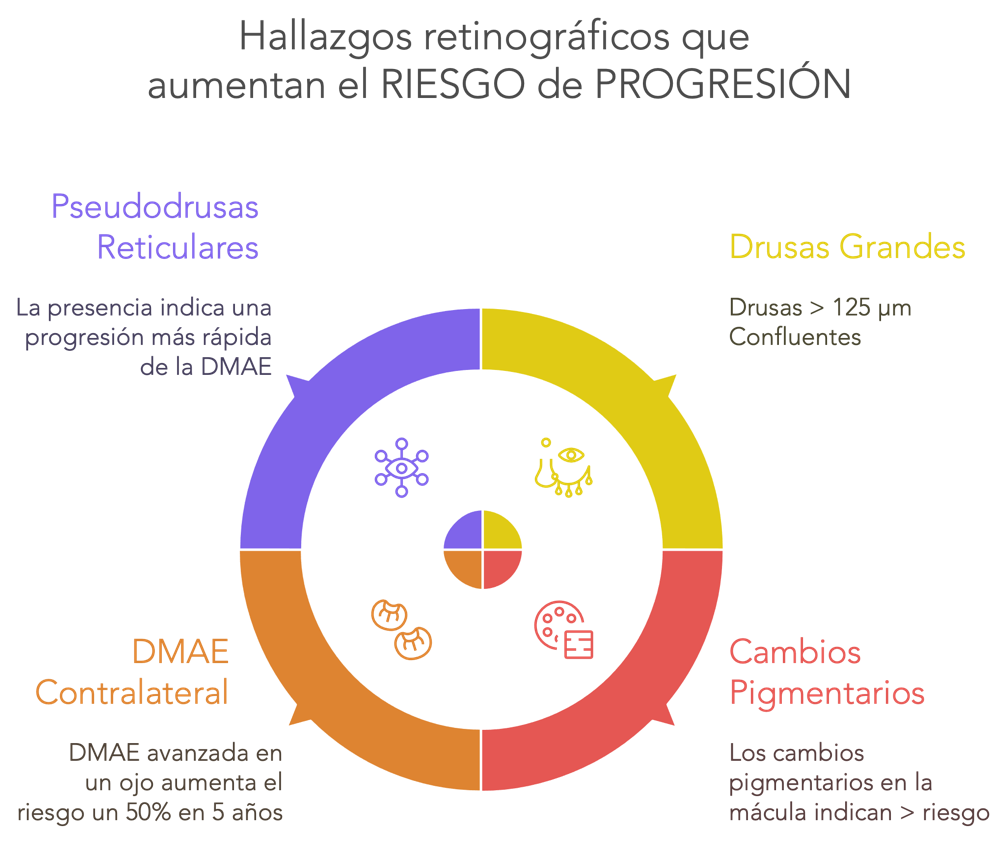
Factores oculares de riesgo
- Drusas grandes (>125 μm), especialmente confluentes [3]
- Alteraciones pigmentarias del EPR (hipo/hiperpigmentación macular) [3]
- DMAE avanzada contralateral: riesgo del 43% a 5 años en el ojo adelfo [12]
- Pseudodrusas reticulares (drusas subretinianas): asociadas con progresión más rápida tanto a atrofia geográfica como a forma neovascular [6]
Profundización sobre genética de DMAE y scores de riesgo poligénico en la Guía Avanzada de DMAE.
Clasificación clínica
La clasificación clínica simplificada, basada en los criterios de Beckman/Ferris [3] y en los hallazgos del AREDS [4], sigue siendo la más operativa para la toma de decisiones en la práctica optométrica. La clave está en asociar cada categoría con un protocolo de acción concreto.
Clasificación por estadio y riesgo de progresión
| Estadio | Hallazgos clínicos | Riesgo 5a | AV típica | Seguimiento |
| Envejecimiento normal | Solo drusas pequeñas (<63 μm, druplets) | <1% | Normal | Rutinario |
| DMAE temprana | Drusas medianas (≥63 a <125 μm) sin alteraciones pigmentarias significativas | ~3% | ≥20/32 | Anual |
| DMAE intermedia | Drusas grandes (≥125 μm) o drusas medianas + alteraciones pigmentarias del EPR | 12-25% | Variable | Semestral |
| DMAE avanzada seca | Atrofia geográfica del EPR. Pérdida de fotorreceptores. Progresión lenta pero irreversible | N/A | Según AG | 3-6 meses |
| DMAE avanzada húmeda | NVC activa: exudación, hemorragias, desprendimiento de EPR o neurosensorial. Progresión rápida sin tratamiento | N/A | Variable | URGENTE |
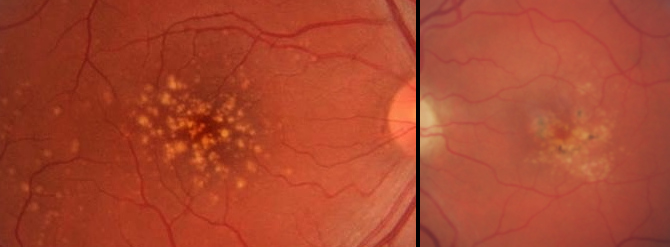
DMAE intermedia
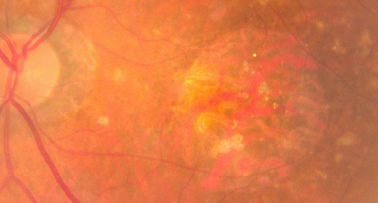
DMAE avanzada atrófica
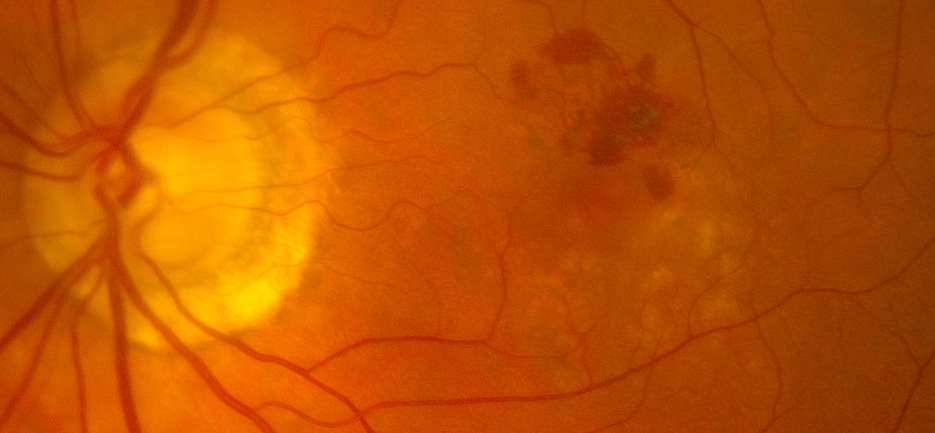
DMAE avanzada neovascular
Riesgo de progresión a DMAE avanzada en 5 años (AREDS)
El riesgo se estratifica según la presencia de drusas grandes y alteraciones pigmentarias, considerando ambos ojos:
| Factores de riesgo presentes | Riesgo a 5 años | Acción |
| 0 factores (sin drusas grandes ni alt. pigmentarias) | 0,5% | Seguimiento anual |
| 1 factor (drusas grandes O alt. pigmentarias, un ojo) | 3% | Seguimiento anual |
| 2 factores | 12% | AREDS2 + semestral |
| 3 factores | 25% | AREDS2 + semestral |
| 4 factores (ambos ojos afectados) | 50% | AREDS2 + trimestral |
Clasificación por localización
- Subfoveal: afectación directa de la fóvea. Mayor impacto en AV central
- Yuxtafoveal: lesión a 1-199 μm del centro foveal. Amenaza inminente
- Extrafoveal: lesión a ≥200 μm del centro. Menor impacto inmediato, pero requiere vigilancia
Protocolo de evaluación optométrica
La evaluación de un paciente con sospecha de DMAE requiere un enfoque sistemático que combine anamnesis dirigida, pruebas funcionales y evaluación morfológica. Muchos pacientes en estadios iniciales mantienen agudeza visual normal en consulta, pero experimentan dificultades significativas en su vida diaria.
Anamnesis dirigida
La historia clínica debe enfocarse en síntomas específicos de disfunción macular:
- Metamorfopsias (líneas onduladas, imágenes distorsionadas)
- Micropsias/macropsias (alteración del tamaño percibido de objetos)
- Dificultad para leer, reconocer caras, conducir, usar dispositivos electrónicos
- Necesidad de mayor iluminación para tareas de cerca
- Escotomas centrales o zonas borrosas/oscuras en el campo visual
- Evolución temporal: cambios agudos (días) pueden indicar conversión a forma neovascular. Urgencia en la anamnesis
- Historia familiar de DMAE (primer grado: riesgo x3-6)
Pruebas optométricas
Agudeza Visual
- AV de lejos con mejor corrección (ETDRS preferiblemente, o Snellen)
- AV de cerca con adición apropiada
- AV con agujero estenopeico (descartar componente refractivo)
- Evaluación en condiciones de baja iluminación
- AV con corrección óptima y filtros selectivos
- Documentar asimetría entre ojos y cambios progresivos
Sensibilidad al Contraste
- Especialmente sensible en estadios tempranos (puede alterarse antes que la AV)
- Test Pelli-Robson o sistemas digitales
- Evaluar en diferentes frecuencias espaciales
- Correlaciona mejor con función visual real que la AV estándar
Test de Amsler
- Evaluación monocular a 30 cm con corrección de cerca
- Selección de rejilla adecuada según caso clínico
- Documentar metamorfopsias, escotomas y distorsiones (localización y extensión)
- Educación del paciente para automonitorización domiciliaria (fundamental)
- Limitación: baja sensibilidad para DMAE temprana
Oftalmoscopía y Retinografía
- Biomicroscopía: Examen estereoscópico de mácula con lente de +78D o +90D
- Retinografía: documentación objetiva para seguimiento longitudinal
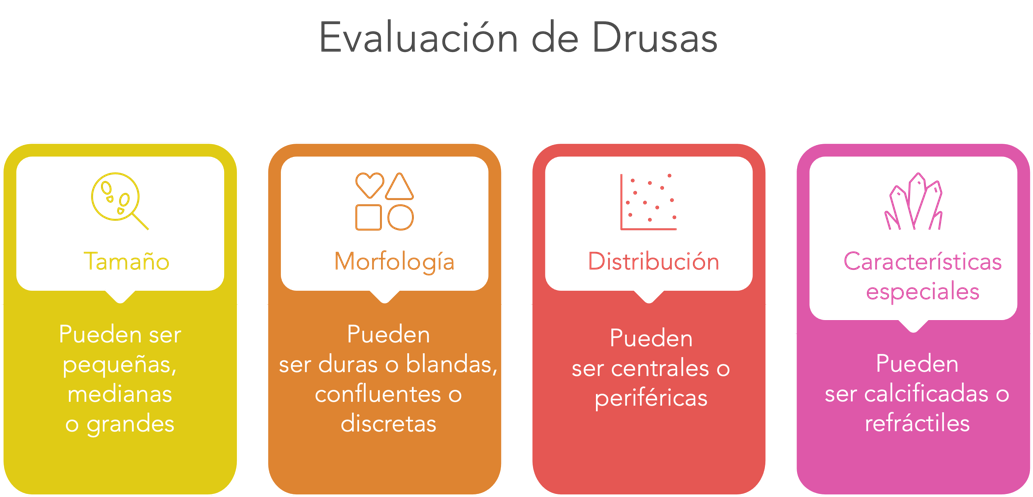
- Identificación y clasificación de drusas (tamaño, distribución, confluencia, tipo)
- Evaluación de alteraciones pigmentarias del EPR y áreas de atrofia
- Detección de signos de neovascularización (exudados, hemorragias)
- Comparación con exámenes previos para detectar progresión
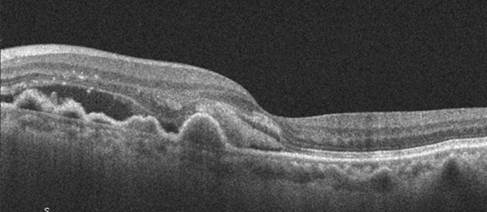
OCT Macular
- Evaluación estructural de drusas, EPR, capas retinianas externas
- Detección de fluido intra/subretiniano (signo de actividad neovascular)
- Monitorización cuantitativa de la progresión (mapas de grosor, volúmenes)
- Comparación con exámenes previos (herramienta de seguimiento esencial)
Autofluorescencia del Fondo (FAF)
Herramienta esencial en DMAE atrófica. Muestra áreas hipoautofluorescentes correspondientes a atrofia geográfica y bordes hiperautofluorescentes que indican progresión activa.
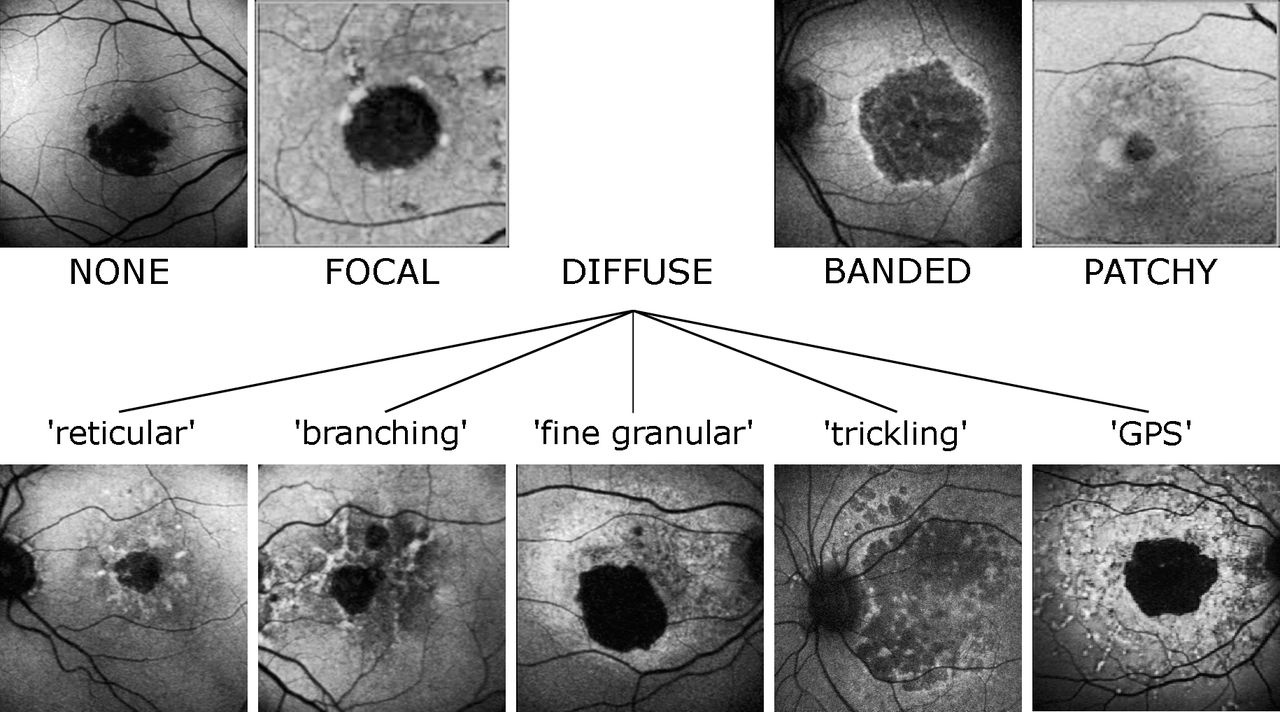
Los patrones de FAF se correlacionan con tasas de crecimiento de AG de 1-2 mm²/año (Holz et al., 2017).
OCT-Angiografía (OCT-A)
Tecnología cada vez más accesible. Permite detectar neovascularización coroidea sin necesidad de inyección de contraste, lo que la convierte en una herramienta de cribado no invasiva de alto valor.
La OCT-A detecta neovascularización tipo 1 subclínica (asintomática) en aproximadamente el 14% de ojos clasificados como DMAE intermedia mediante retinografía convencional. Profundización en la Guía Avanzada.
Monitorización domiciliaria digital
Las aplicaciones móviles de monitorización (como Alleye, myVisionTrack o ForeseeHome) complementan o mejoran la detección de cambios respecto al test de Amsler en papel, con mayor sensibilidad y registro objetivo de datos.
ForeseeHome detectó conversión a DMAE húmeda con AV ≥20/40 en el 94% de los casos frente al 62% con Amsler convencional (estudio HOME, JAMA Ophthalmology 2014). Más detalles en la Guía Avanzada.
Manejo y seguimiento optométrico
El manejo optométrico de la DMAE combina seguimiento estructurado por estadio, intervenciones nutricionales basadas en evidencia, modificación de factores de riesgo y rehabilitación visual. Los pacientes informados sobre su condición y con protocolos de automonitorización domiciliaria obtienen mejores resultados funcionales a largo plazo.
Protocolo de seguimiento por estadio
DMAE TEMPRANA - Seguimiento anual
- Retinografía + OCT macular (si disponible) como baseline
- Educación sobre factores de riesgo modificables (tabaco, dieta, UV)
- Enseñanza de test de Amsler para uso domiciliario
- Valorar suplementación AREDS2 si factores de riesgo adicionales
DMAE INTERMEDIA - Seguimiento semestral
- Retinografía + OCT macular cada 6 meses
- Suplementación AREDS2 (si indicada)
- Evaluación funcional detallada (SC, Amsler, AV en condiciones diversas)
- Educación específica sobre síntomas de alarma de conversión húmeda
- Considerar monitorización domiciliaria digital
DMAE AVANZADA - Seguimiento conjunto con oftalmología
- Forma atrófica:
- Monitorización de progresión de atrofia (FAF + OCT) cada 3-6 meses
- Vigilancia de desarrollo de forma neovascular en ambos ojos
- Rehabilitación visual, ayudas ópticas y apoyo psicosocial
- Forma neovascular:
- Frecuencia según protocolo de tratamiento anti-VEGF del oftalmólogo
- Monitorización de AV, función central y respuesta al tratamiento
- Rehabilitación visual, ayudas ópticas y apoyo psicosocial
Suplementación nutricional AREDS2
- Indicación: DMAE intermedia o avanzada en al menos un ojo [4]
- Beneficio: reducción del 25% en riesgo de progresión a formas avanzadas [4]
- Contraindicación: evitar betacaroteno en fumadores y exfumadores recientes (riesgo aumentado de cáncer de pulmón). La fórmula AREDS2 sustituye betacaroteno por luteína/zeaxantina [9]
Ayudas ópticas y rehabilitación visual
- Magnificación óptica: lupas manuales, lupas con soporte, telescopios
- Filtros selectivos para mejora de contraste y control de deslumbramiento
- Sistemas de magnificación electrónicos: CCTV, tablets, dispositivos portátiles
- Ayudas basadas en inteligencia artificial (dispositivos de asistencia visual)
- Mejora de iluminación ambiental y ergonómica visual
- Entrenamiento en técnicas de visión excéntrica (PRL: Preferred Retinal Locus) [11]
Profundización sobre rehabilitación visual avanzada, selección de ayudas y dispositivos con IA en la Guía de Baja Visión en www.farobajavision.com.
Señales de alarma y criterios de derivación
La derivación oportuna al oftalmólogo especialista en retina es el aspecto más crítico del manejo optométrico de DMAE. La comunicación con el especialista debe incluir evolución temporal de síntomas, hallazgos específicos, imágenes de OCT/retinografía y cualquier cambio reciente en la función visual.
Derivación urgente (24-48 horas)
- Pérdida visual aguda o subaguda (días a semanas)
- Metamorfopsias de nueva aparición o empeoramiento súbito
- Escotomas centrales de aparición reciente
- Hemorragias retinianas o subretinianas nuevas
- Exudados duros de nueva aparición
- Desprendimiento del EPR o neurosensorial
- Cualquier signo sugestivo de neovascularización coroidea
Derivación preferente (2-4 semanas)
- Progresión documentada de drusas o alteraciones pigmentarias
- Drusas grandes blandas confluentes de reciente aparición
- Disminución progresiva de AV no explicada por otros factores
- Desarrollo de atrofia geográfica
- Paciente candidato a ensayos clínicos
Criterios en el tratamiento oftalmológico (información para el optometrista)
- Anti-VEGF: neovascularización coroidea activa con afectación o amenaza foveal. Fármacos actuales: ranibizumab, aflibercept, brolucizumab, faricimab [7, 8]
- Atrofia geográfica: nuevas terapias aprobadas (pegcetacoplan, avacincaptad pegol) que ralentizan la progresión de la AG [6]
- Edema macular secundario: anti-VEGF, corticoides intravítreos [8]
Genética de la DMAE y tablas de riesgo en la Guía Avanzada de DMAE.
Derivación a otros profesionales
- Especialista en baja visión y rehabilitación visual: DMAE avanzada con limitación funcional significativa
- Psicólogo: ansiedad o depresión relacionada con pérdida visual
- Trabajador social: necesidad de adaptaciones domiciliarias o apoyo social
- Nutricionista: optimización de dieta antioxidante y suplementación
Herramientas tecnológicas en el manejo de DMAE
La integración de tecnología avanzada en la práctica optométrica ha transformado la capacidad de detección precoz y seguimiento de la DMAE. A continuación, se presentan las herramientas clave con su aportación clínica específica:
Profundización en inteligencia artificial aplicada, telediagnóstico y tecnología de cribado remoto en la Guía Avanzada de Tecnología en Optometría.
Consideraciones especiales
DMAE y conducción
Los pacientes con DMAE pueden mantener el permiso de conducir si cumplen los requisitos visuales legales. Sin embargo, la sensibilidad al contraste reducida y los escotomas centrales pueden comprometer significativamente la seguridad vial incluso con agudeza visual aparentemente adecuada. Es necesaria una evaluación funcional realista, no solo la medición de AV estándar.
DMAE unilateral vs. bilateral
Los pacientes con DMAE avanzada unilateral presentan un riesgo del 43% a 5 años de desarrollar DMAE avanzada en el ojo contralateral [12]. El seguimiento debe intensificarse (cada 3-4 meses) con educación específica sobre síntomas de alarma. La automonitorización con test de Amsler es especialmente crítica en estos pacientes.
Aspectos psicosociales
La DMAE avanzada tiene un impacto profundo en la calidad de vida: depresión, aislamiento social y pérdida de independencia. El optometrista debe evaluar activamente estos aspectos y facilitar el acceso a recursos de apoyo psicológico, social y de rehabilitación funcional.
Prevención primaria
Aunque no es posible prevenir completamente la DMAE, la educación sobre factores de riesgo modificables (tabaquismo, dieta, protección UV, control cardiovascular), especialmente en pacientes con historia familiar, puede influir significativamente en la progresión a largo plazo.
Checklist para la práctica clínica
Resumen operativo de acciones clave:
- Realizar anamnesis dirigida a síntomas maculares en todo paciente >50 años
- Clasificar el estadio de DMAE y estratificar riesgo de progresión (AREDS). Oftalmólogo
- Documentar hallazgos con retinografía y OCT (baseline imprescindible)
- Enseñar test de Amsler a TODO paciente con DMAE para automonitorización domiciliaria
- Indicar suplementación AREDS2 en DMAE intermedia y avanzada (sin betacaroteno en fumadores)
- Educar sobre factores de riesgo modificables: tabaco, dieta, UV, riesgo CV
- Derivar urgente (24-48 h) ante cualquier sospecha de conversión a DMAE neovascular
- Establecer seguimiento individualizado según estadio y riesgo
- Evaluar aspectos psicosociales y derivar a rehabilitación visual cuando sea necesario
- Mantener comunicación detallada con el oftalmólogo: síntomas, imágenes, evolución

Este documento es informativo y no sustituye ni a una consulta médica ni optométrica. El diagnóstico definitivo y el plan de tratamiento deben ser efectuados, según el caso, por su oftalmólogo o por su optometrista.
Referencias bibliográficas
- Wong WL, Su X, Li X, et al. (2014). Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040. Lancet Global Health, 2(2), e106-116.
- Klein R, Chou CF, Klein BE, et al. (2011). Prevalence of age-related macular degeneration in the US population. Arch Ophthalmol, 129(1), 75-80.
- Ferris FL, Wilkinson CP, Bird A, et al. (2013). Clinical classification of age-related macular degeneration. Ophthalmology, 120(4), 844-851.
- Age-Related Eye Disease Study 2 Research Group. (2013). Lutein + zeaxanthin and omega-3 fatty acids for AMD. JAMA, 309(19), 2005-2015.
- Chakravarthy U, Wong TY, Fletcher A, et al. (2010). Clinical risk factors for AMD: a systematic review and meta-analysis. BMC Ophthalmol, 10, 31.
- Holz FG, Strauss EC, Schmitz-Valckenberg S, et al. (2014). Geographic atrophy: clinical features and potential therapeutic approaches. Ophthalmology, 121(5), 1079-1091.
- Rosenfeld PJ, Brown DM, Heier JS, et al. (2006). Ranibizumab for neovascular AMD. NEJM, 355(14), 1419-1431.
- Schmidt-Erfurth U, Chong V, Loewenstein A, et al. (2014). Guidelines for management of neovascular AMD (EURETINA). Br J Ophthalmol, 98(9), 1144-1167.
- Evans JR, Lawrenson JG. (2017). Antioxidant vitamin and mineral supplements for preventing AMD. Cochrane Database Syst Rev, 7, CD000253.
- Chew EY, Clemons TE, SanGiovanni JP, et al. (2014). Secondary analyses of lutein/zeaxanthin on AMD progression. JAMA Ophthalmol, 132(2), 142-149.
- Sunness JS, Gonzalez-Baron J, Applegate CA, et al. (1999). Enlargement of atrophy and visual acuity loss in geographic atrophy form of AMD. Ophthalmology, 106(9), 1768-1779.
- Klein R, Klein BE, Knudtson MD, et al. (2007). Fifteen-year cumulative incidence of AMD. Ophthalmology, 114(2), 253-262.
- Augood CA, Vingerling JR, de Jong PT, et al. (2006). Prevalence of age-related maculopathy in older Europeans: the European Eye Study (EUREYE). Arch Ophthalmol, 124(4), 529-535.
- AREDS2-HOME Study Research Group. (2014). Randomized trial of a home monitoring system for early detection of choroidal neovascularization. JAMA Ophthalmol, 132(3), 258-264.