MINIGUÍA CLÍNICA
Edema Macular Diabético (EMD)
Ficha rápida
El oftalmólogo es quien diagnostica y trata el EMD. El optometrista debe tener conocimientos sobre el EMD para derivar los casos sospechosos.
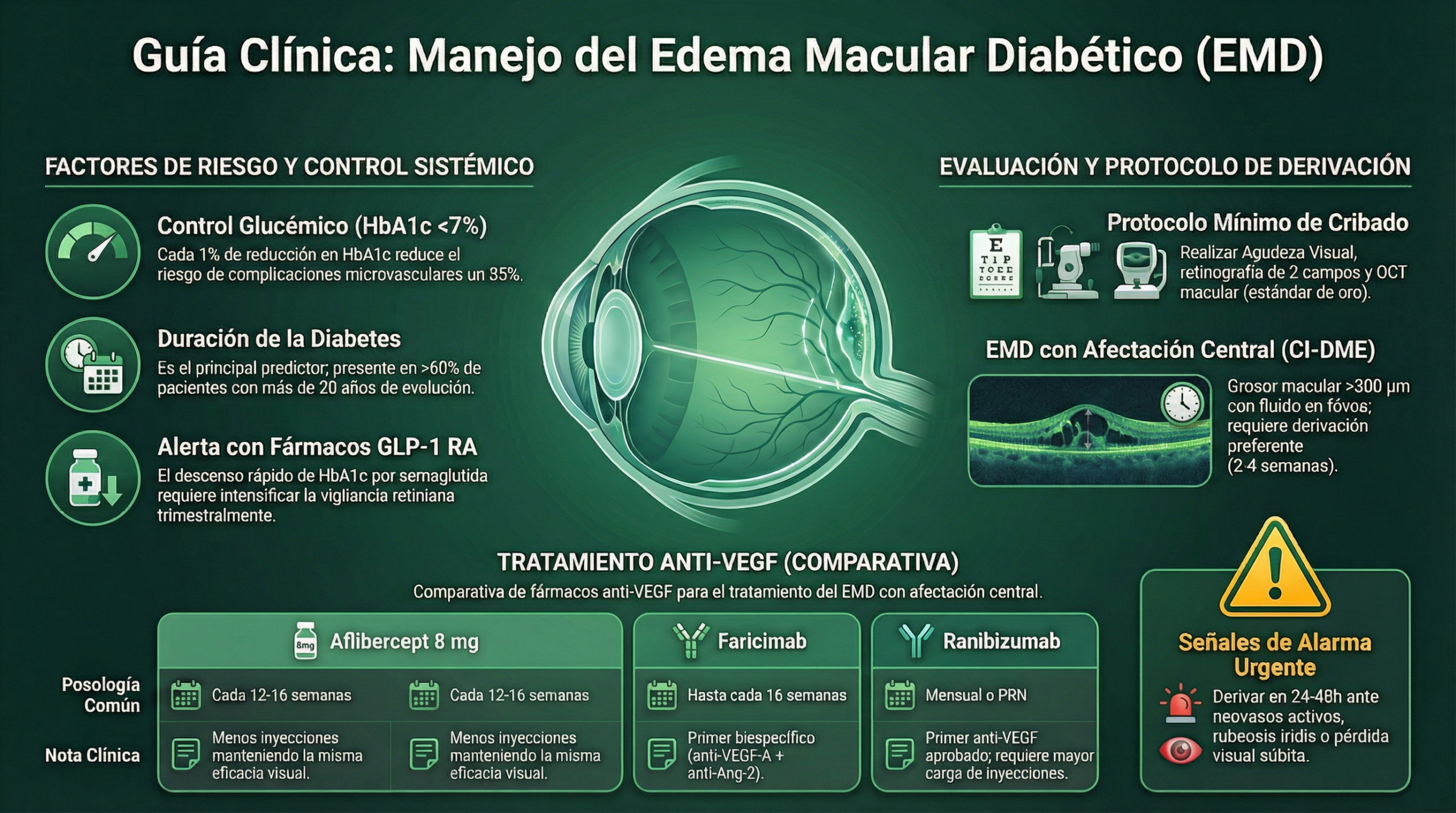
Factores de riesgo
La identificación y control de los factores de riesgo modificables es fundamental para prevenir la aparición y progresión del EMD. El optometrista debe conocerlos para educar al paciente y comunicarse eficazmente con endocrinología y atención primaria.
Factores principales
Factores adicionales
Los agonistas GLP-1 (semaglutida, liraglutida) están en auge por la epidemia de obesidad y DM2. El optometrista debe saber que un descenso rápido de HbA1c (>2% en 6 meses) puede empeorar transitoriamente la RD. No es motivo para suspender el fármaco, pero sí para intensificar el seguimiento ocular.
Clasificación del EMD
La clasificación del EMD ha evolucionado de la evaluación clínica (ETDRS) a la valoración por OCT. Ambas son complementarias.
Clasificación anatómica por OCT
Patrones morfológicos en OCT
- Engrosamiento espongiforme difuso: Líquido intrarretiniano (IRF) en espacios quistóides en capas externas. Patrón más frecuente
- Edema quistóideo (EMQ): Cavidades quistóides bien definidas, frecuentemente en capas nucleares interna y externa. Indicador de cronicidad
- Desprendimiento seroso del neuorepitelio (SRF): Líquido subretiniano bajo la fovea. Puede indicar mayor actividad inflamatoria
- Tracción vitreomacular (TVM): Membrana epirretiniana o adherencia vitreoafoveal que tracciona y mantiene el edema. Puede requerir vitrectomía
- Alteración de la zona elípsoide (EZ) e integridad de la membrana limitante externa (ELM): Marcadores pronósticos de recuperación visual. Disrupción = peor pronóstico funcional
El OCT es el estándar para diagnóstico, clasificación y seguimiento del EMD. El optometrista que realiza OCT macular y retinografía en pacientes diabéticos es un agente clave de detección precoz. El EMD subclínico detectable por OCT precede a la pérdida visual en meses o años.
Protocolo de evaluación optométrica
El cribado de RD y EMD es una de las intervenciones más coste-efectivas en salud pública. El optometrista puede y debe ser el primer filtro diagnóstico [6].
Anamnesis dirigida
- Tipo de diabetes, duración, última HbA1c: datos fundamentales para estratificar riesgo
- Control metabólico: adherencia a tratamiento, cambios recientes de medicación (inicio de GLP-1 RA, insulinización)
- Comorbilidades: HTA, dislipemia, nefropatía, embarazo, apnea del sueño
- Síntomas visuales: visión borrosa fluctuante, metamorfopsia, escotoma central
- Historial ocular: cirugía de catarata reciente, inyecciones intravítreas previas, láser previo
Evaluación clínica
Agudeza visual
- AVMC lejos y cerca. Documentar cambios respecto a visitas previas. La visión puede fluctuar con los niveles de glucemia
Retinografía
- Mínimo: 2 campos (centrado en mácula + centrado en papila). Ideal: retinografía de campo ultrapanorámico
- Clasificar la RD según escala ICDR: ausente, leve, moderada, severa, proliferativa
- Buscar: microaneurismas, hemorragias, exudados duros (especialmente en anillo circinar perifoveal), exudados algodonosos, arrosariamiento venoso, AMIR, neovasos
OCT macular
- Gold standard para detectar y cuantificar EMD. Medir CST (grosor subfoveal central). Identificar fluido intrarretiniano, subretiniano, quistes
- Evaluar integridad de la zona elipsoide (EZ) y membrana limitante externa (ELM): marcadores pronósticos de AV final
- Descartar tracción vitreomacular asociada
- Mapas de grosor macular: comparar con visitas previas para detectar cambios subclínicos
OCT-Angiografía (si disponible)
- Visualiza la microvasculatura retiniana sin contraste: detección de zonas de no perfusión, microaneurismas, área de zona avascular foveal (FAZ) aumentada
- Complementaria a la retinografía para evaluar isquemia macular
Tonometría
- Descartar glaucoma concurrente (prevalencia aumentada en diabéticos). Los corticoides intravítreos elevan PIO
Protocolo mínimo para cribado de RD/EMD en optometría: AVMC + retinografía 2 campos + OCT macular. Si dispone de OCT-A, añadirlo en pacientes con RD moderada-severa. Derivar con toda esta información permite al oftalmólogo tomar decisiones rápidas y reduce tiempos de espera del sistema.
Manejo terapéutico del EMD
El tratamiento del EMD ha cambiado radicalmente en las últimas dos décadas. El optometrista no trata directamente, pero necesita conocer las opciones para educar al paciente, reforzar adherencia al tratamiento y detectar signos de respuesta insuficiente [2, 6, 9, 10].
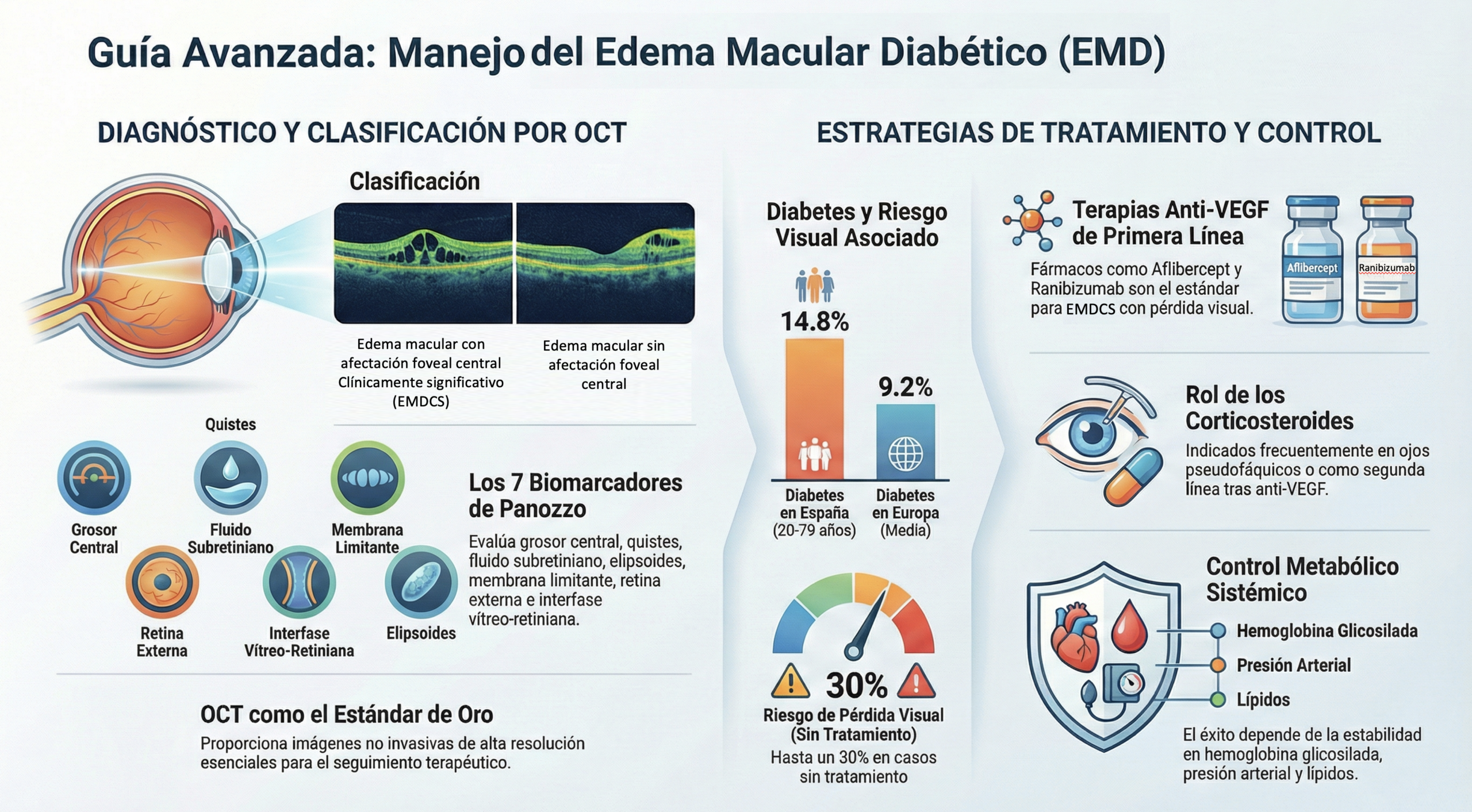
Control sistémico (transversal a todo estadio)
BASE: Control Metabólico y Cardiovascular
- HbA1c <7% (objetivo individualizado según comorbilidades). Cada 1% de reducción = ~35% menos complicaciones microvasculares (UKPDS, DCCT)
- TA <130/80 mmHg. Reducción de progresión de RD ~34% con control estrictoLDL <100 mg/dL. Fenofibrato considerado para reducción de progresión de RD (FIELD, ACCORD-Eye)
- Cese tabaquismo. Ejercicio regular. Dieta mediterránea
- Derivar a endocrinología si control metabólico suboptimal
Terapias específicas para el EMD
Anti-VEGF intravítreo (estándar de cuidado para CI-DME)
Corticoides intravítreos (segunda línea o EMD refractario)
Láser
- Láser focal/grid (ETDRS): históricamente el estándar. Hoy desplazado por anti-VEGF como primera línea en CI-DME. Aún indicado en EMD no central con exudados focales amenazantes
- Láser micropulsado subumbral: alternativa con menor daño tisular. Evidencia creciente como terapia combinada o de mantenimiento. No destruye fotorreceptores
~30-40% de los pacientes con EMD son refractarios al anti-VEGF estándar (~20% persisten con edema tras 36 meses de inyecciones mensuales). Las opciones incluyen: switch a faricimab o aflibercept 8 mg, añadir/cambiar a corticoide intravítreo, o combinación anti-VEGF + corticoide. El optometrista detecta la falta de respuesta en el seguimiento OCT.
Señales de alarma y criterios de derivación
El optometrista es frecuentemente el primer profesional en detectar signos de glaucoma. La derivación oportuna y la comunicación detallada con el oftalmólogo son determinantes para el pronóstico visual.
Derivación urgente (24-48 horas)
- RD proliferativa activa: neovasos en disco o retina, hemorragia vítrea o prerretiniana
- Pérdida visual súbita en paciente diabético (hemorragia vítrea, desprendimiento de retina traccional, isquemia macular aguda)
- Rubeosis iridis / glaucoma neovascular
- EMD con pérdida visual significativa aguda (≥2 líneas en ≤1 mes)
Derivación preferente (2-4 semanas)
- EMD con afectación central (CI-DME) detectado por OCT, independientemente de la AV
- RD severa no proliferativa (regla 4:2:1): alto riesgo de progresión a proliferativa
- Exudados duros en anillo circinar con amenaza foveal
- Progresión de RD significativa entre visitas de seguimiento
- Paciente en tratamiento intravítreo con respuesta insuficiente detectada en OCT de control
Seguimiento optométrico activo (no derivar, vigilar)
- RD leve-moderada sin EMD: retinografía + OCT cada 12 meses
- RD moderada con EMD subclínico (sin afectación central): OCT cada 3-4 meses. Retinografía cada 6 meses
- Diabético sin RD: cribado anual (puede espaciarse a 2 años si buen control metabólico y duración <10 años)
- Post-tratamiento intravítreo estabilizado: seguimiento OCT según pauta del oftalmólogo tratante
Herramientas tecnológicas
El telediagnóstico de OCT macular y retinografía realizado por optometristas clínicos permite cribado de RD/EMD en pacientes que no llegarían al oftalmólogo hasta tener síntomas. Este modelo de atención primaria visual es coste-efectivo y reduce la ceguera prevenible. Profundización en la Guía Avanzada de Tecnología en Optometría.
Consideraciones especiales
EMD y cirugía de catarata
La facoemulsificación puede empeorar el EMD preexistente o desencadenarlo. En pacientes con RD, se recomienda: estabilizar el EMD con anti-VEGF antes de la cirugía, considerar inyección intravítrea periquirúrgica, y seguimiento OCT postoperatorio estrecho (1, 3 y 6 meses) [2].
EMD en el embarazo
Las diabéticas pregestacionales (tipo 1 y 2) tienen riesgo de progresión rápida de RD/EMD durante el embarazo, especialmente si el control glucémico se intensifica bruscamente. El anti-VEGF está contraindicado en embarazo (riesgo teratogénico teórico). Láser focal puede realizarse si es necesario. Examen al inicio, cada trimestre y a los 3 meses postparto [2].
EMD y GLP-1 RA (semaglutida)
El uso creciente de agonistas GLP-1 (semaglutida, liraglutida, dulaglutida) para DM2 y obesidad requiere atención. Un descenso rápido de HbA1c (>2% en 6 meses) puede empeorar transitoriamente la RD. No se debe suspender el fármaco, pero sí intensificar la vigilancia retiniana (OCT + retinografía cada 3 meses durante el primer año de tratamiento) [8].
Adherencia al tratamiento intravítreo
La carga de inyecciones intravítreas es una barrera principal para la adherencia. Los regimenes TAE (treat-and-extend) y los fármacos de mayor durabilidad (aflibercept 8 mg, faricimab) buscan reducirla. El optometrista que realiza el seguimiento OCT puede reforzar la importancia de completar las cargas de tratamiento y detectar pérdida de seguimiento.
Comunicación interdisciplinar
El informe optométrico de derivación por RD/EMD debe incluir como mínimo: AV actual, clasificación de RD (ICDR), CST por OCT, presencia/ausencia de fluido IRF/SRF, y datos de control metabólico conocidos (HbA1c, TA). Esta información permite al oftalmólogo tomar decisiones sin repetir pruebas y reduce tiempos de espera.
Checklist para la práctica clínica
- Preguntar a TODO paciente diabético: tipo, duración, última HbA1c, medicación actual, comorbilidades (HTA, nefropatía)
- Cribado anual: AVMC + retinografía (mínimo 2 campos) + OCT macular bilateral
- Clasificar la RD según escala ICDR en cada visita. Documentar cambios entre visitas
- Medir CST en OCT macular y comparar con valores previos. Identificar fluido IRF/SRF
- Evaluar integridad de EZ y ELM en OCT (factores pronósticos de recuperación visual)
- Derivar CI-DME (EMD con afectación central) SIEMPRE, independientemente de la AV
- Educar al paciente: “el control de azúcar, tensión y colesterol protege sus ojos”. Reforzar adherencia
- Si inicio reciente de GLP-1 RA (semaglutida): intensificar vigilancia retiniana los primeros 12 meses
- En informe de derivación incluir: AV, clasificación RD, CST, fluido IRF/SRF, HbA1c conocida
- Derivación URGENTE ante: neovasos activos, hemorragia vítrea, rubeosis iridis, pérdida visual súbita
Este documento es informativo y no sustituye ni a una consulta médica ni optométrica. El diagnóstico definitivo y el plan de tratamiento deben ser efectuados, según el caso, por su oftalmólogo o por su optometrista.
Referencias bibliográficas
- Lee R, Wong TY, Sabanayagam C. (2015). Epidemiology of diabetic retinopathy, diabetic macular edema and related vision loss. Eye Vis, 2, 17.
- Wong TY, Sun J, Kawasaki R, et al. (2018). Guidelines on Diabetic Eye Care: ICO Recommendations for Screening, Follow-up, Referral, and Treatment Based on Resource Settings. Ophthalmology, 125(10), 1608-1622.
- GlobalData (2024). Diabetic Macular Edema: Epidemiology Forecast to 2034. ~2.9M diagnosed cases in 7MM.
- Li JQ, Welchowski T, Schmid M, et al. (2020). Prevalence, incidence and future projection of diabetic eye disease in Europe: systematic review and meta-analysis. Eur J Epidemiol, 35(1), 11-23.
- Romero-Aroca P, de la Riva-Fernandez S, Valls-Mateu A, et al. (2016). Changes observed in diabetic retinopathy: eight-year follow-up of a Spanish population. Br J Ophthalmol, 100(10), 1366-1371.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F, et al. (2017). Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica, 237(4), 185-222.
- UK Prospective Diabetes Study (UKPDS) Group. (1998). Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet, 352, 837-853.
- Marso SP, Bain SC, Consoli A, et al. (2016). Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. SUSTAIN-6. N Engl J Med, 375(19), 1834-1844.
- Heier JS, Khanani AM, et al. (2022). Efficacy, Durability, and Safety of Intravitreal Faricimab up to Every 16 Weeks for Neovascular AMD (TENAYA and LUCERNE). Ophthalmology, 129(1), 80-89.
- Brown DM, Emanuelli A, Bandello F, et al. (2022). KESTREL and KITE: 52-Week Results from Two Phase III Pivotal Trials of Brolucizumab for Diabetic Macular Edema. Am J Ophthalmol, 238, 157-172.
- Wykoff CC, Brown DM, et al. (2023). Aflibercept 8 mg for DME: PHOTON Phase 2/3 trial. Lancet, 402(10418), 2254-2265.
- Friedman SM, Xu Y, et al. (2025). Aflibercept 8 mg vs Faricimab T&E for DME: Bayesian NMA. Ophthalmol Ther, 14(11), 2919-2936.