MINIGUÍA CLÍNICA
Glaucoma
Guía práctica para optometristas
Ficha rápida
El oftalmólogo es quien diagnostica y trata el glaucoma. El optometrista debe tener conocimientos sobre el glaucoma para derivar los casos sospechosos.
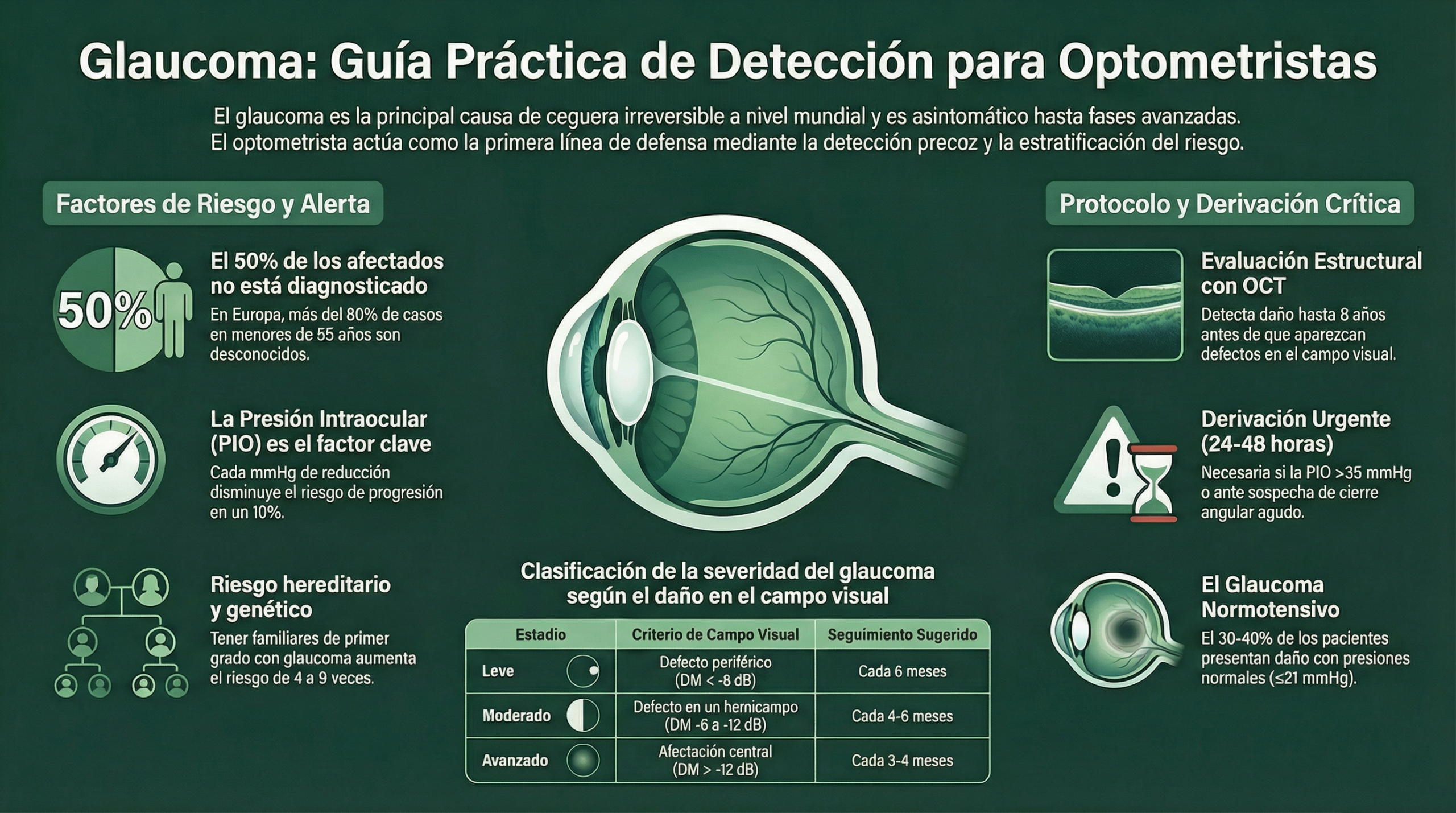
Factores de riesgo
La estratificación del riesgo de glaucoma permite optimizar los protocolos de cribado y la frecuencia de seguimiento. El riesgo aumenta de forma multiplicativa con la combinación de factores.
Factores principales
Factores adicionales
Profundización sobre genética del glaucoma, síndromes pseudoexfoliativos y factores vasculares en la Guía Avanzada de Glaucoma.
Clasificación clínica
La clasificación del glaucoma se basa en la anatomía del ángulo camerular (abierto vs cerrado), la etiología (primario vs secundario) y la edad de aparición. El optometrista debe conocer los tipos de glaucoma para orientar la derivación y el manejo apropiados.
Clasificación principal
Estadificación por severidad (basada en campo visual)
La gonioscopía por parte del oftalmólogo es imprescindible para clasificar correctamente el tipo de glaucoma. Más del 50% de los glaucomas de ángulo cerrado crónicos pueden confundirse con GPAA sin una exploración goniscópica adecuada. Profundización en la Guía Avanzada.
Protocolo de evaluación optométrica
La evaluación optométrica del glaucoma integra medidas estructurales y funcionales. El objetivo es detectar daño antes de que el paciente perciba síntomas, ya que la pérdida de campo visual no se manifiesta hasta que se ha perdido un 30-50% de las células ganglionares, y derivar al oftalmólogo para diagnóstico y tratamiento (si procede).
Anamnesis dirigida
- Historia familiar de glaucoma (familiares de primer grado: riesgo x4-9)
- Uso actual o previo de corticoides (tópicos, inhalados, sistémicos)
- Antecedentes oculares: miopía, traumatismos, cirugías, uveítis
- Antecedentes sistémicos: diabetes, HTA, hipotensión nocturna, migraña, apnea del sueño, Raynaud
- Medicación habitual (anticolinérgicos, simpatomiméticos, antidepresivos pueden influir en ángulo)
- Síntomas de cierre angular agudo: dolor ocular intenso, cefalea, náuseas/vómitos, halos alrededor de luces, ojo rojo, visión borrosa súbita
Pruebas optométricas
Tonometría
- Tonometría: tonometría de rebote (iCare), tonometría de contorno dinámico (Pascal), neumotonometría
- La PIO aislada NO diagnostica glaucoma. Rango normal 10-21 mmHg, pero el 30-40% de GPAA tiene PIO ≤21 mmHg
- Considerar variación diurna de PIO (fluctuaciones de 3-6 mmHg son habituales; >8 mmHg es factor de riesgo)
- Interpretar siempre en contexto de paquimetría corneal
Paquimetría corneal
- Medición del espesor corneal central (ECC). Media normal: ~545 μm
- ECC < 520 μm: infraestima PIO real (factor de riesgo independiente, OHTS) [5]
- ECC > 580 μm: puede sobreestimar PIO
- Esencial para interpretar correctamente la tonometría y estratificar riesgo
Gonioscopía y biomicroscopía
- Gonioscopía: La realiza el oftalmólogo. Evaluación directa del ángulo camerular. Imprescindible en toda evaluación de glaucoma
- Biomicroscopía: Van Herick para valoración de la profundidad de la cámara anterior
- Permite identificar: ángulo estrecho/cerrado, pseudoexfoliación, dispersión pigmentaria, neovasos, sinequias
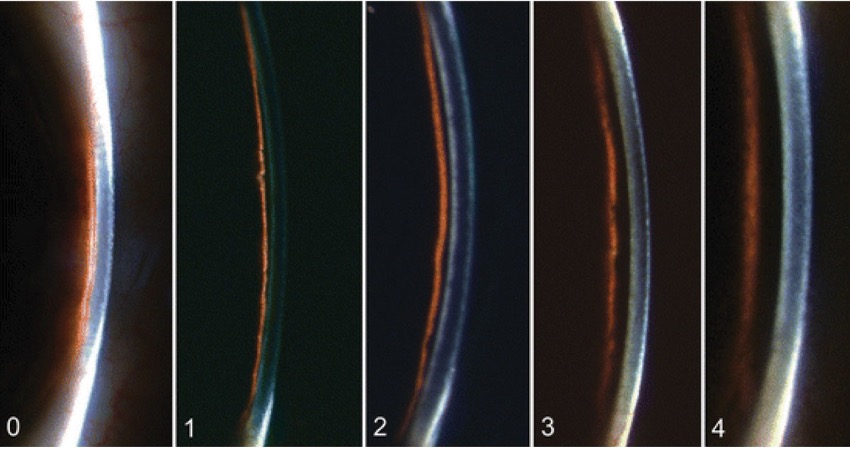
El método Van Herick evalúa la profundidad de la cámara anterior en relación con el grosor de la córnea desde los grados 0 a 4. Fuente
Evaluación del nervio óptico
- Oftalmoscopía/biomicroscopía con lente de +78D/+90D: evaluación estereoscópica del disco
- Valorar: relación excavación/disco (E/D), asimetría E/D entre ojos (>0.2 sospechosa), regla ISNT, muescas (notches), hemorragias en astilla, atrofia peripapilar
- Retinografía: documentación objetiva para seguimiento longitudinal
- La evaluación subjetiva del NO tiene alta variabilidad interobservador. Complementar siempre con OCT
OCT del nervio óptico y capa de fibras nerviosas (CFNR)
- Análisis cuantitativo y reproducible de CFNR peripapilar y complejo de células ganglionares (CCG) macular
- Detección de daño estructural antes de que aparezca defecto campimétrico (hasta 5-8 años antes)
- Mapas de espesor, comparación con base normativa por edad, análisis de progresión longitudinal
- Complementar con análisis de CCG macular: especialmente útil en miopes y glaucoma incipiente
La OCT detecta pérdida de CFNR en estadios preperimétricos (sin defecto de CV) en el 60% de ojos con sospecha de glaucoma. Es la herramienta de detección precoz más potente disponible para el optometrista. Profundización en la Guía Avanzada.
Campimetría (Perimetría estática automatizada)
- Prueba funcional de referencia para confirmar diagnóstico y estadificar severidad
- Protocolos habituales: Humphrey SITA-Standard o SITA-Fast (24-2 o 30-2); Octopus
- Evaluar: desviación media (DM), desviación estándar del modelo (DSM/PSD), índices de fiabilidad
- Defectos típicos: escotoma de Bjerrum, escalón nasal, depresión generalizada, isla temporal
- Se necesitan al menos 2 campos fiables para confirmar un defecto reproducible
- La estrategia 10-2 es esencial en glaucoma avanzado para evaluar visión central residual
Evaluación del ángulo por imagen: OCT de segmento anterior
Alternativa no invasiva a la gonioscopía para la evaluación del ángulo. Permite medir parámetros angulares cuantitativos (AOD, TISA) y detectar configuraciones de riesgo de cierre angular.
La OCT de segmento anterior identifica ángulos susceptibles de cierre en el 12% de pacientes asintomáticos con PIO normal y ángulo aparentemente abierto por Van Herick. Profundización en la Guía Avanzada.
Manejo y seguimiento optométrico
El objetivo del tratamiento del glaucoma es reducir la PIO a un nivel que prevenga daño adicional al nervio óptico (PIO diana). El optometrista desempeña un papel esencial en la detección, el seguimiento longitudinal, la monitorización de la adherencia al tratamiento y la educación del paciente.
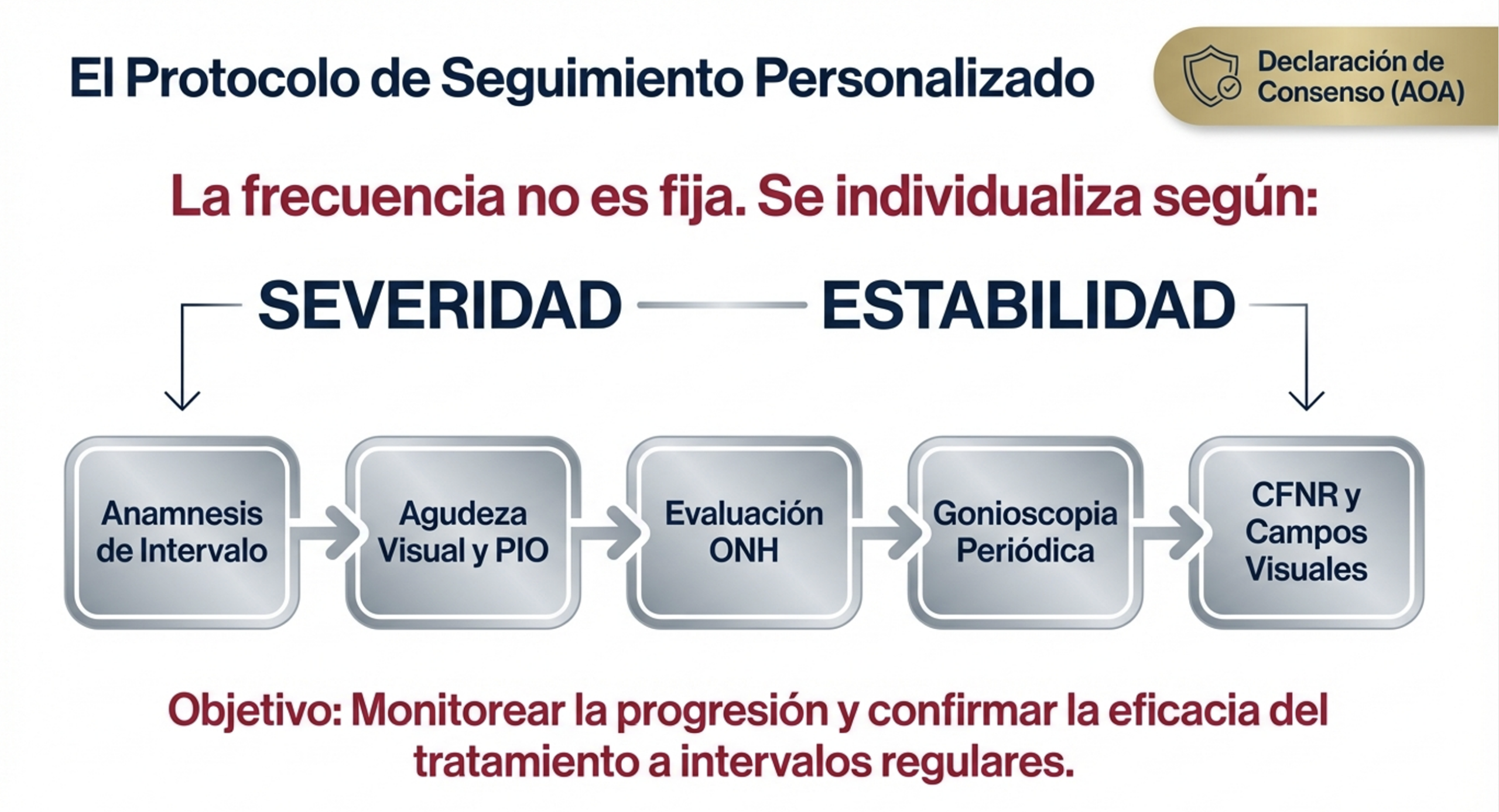
Protocolo de seguimiento por estadio
SOSPECHA DE GLAUCOMA / HTO — Seguimiento cada 6-12 meses
- Tonometría + paquimetría (baseline)
- OCT CFNR + CCG macular como baseline
- Campimetría 24-2 (al menos 2 campos fiables iniciales)
- Gonioscopía (al menos una vez para clasificar ángulo)
- Retinografía del disco óptico
- Educación sobre factores de riesgo y síntomas de alarma
GLAUCOMA LEVE — Seguimiento cada 6 meses
- Tonometría en cada visita (verificar PIO diana)
- OCT CFNR + CCG macular cada 6-12 meses (análisis de progresión)
- Campimetría 24-2 cada 6-12 meses
- Evaluación de adherencia al tratamiento
- Monitorización de efectos adversos de medicación tópica
GLAUCOMA MODERADO-AVANZADO — Seguimiento cada 3-4 meses
- Seguimiento conjunto con oftalmólogo
- Tonometría + evaluación de respuesta al tratamiento
- OCT y campimetría según protocolo del especialista
- Campimetría 10-2 en glaucoma avanzado (visión central)
- Evaluación de calidad de vida y función visual real
- Ayudas de baja visión si procede
- Apoyo psicológico y adaptación funcional
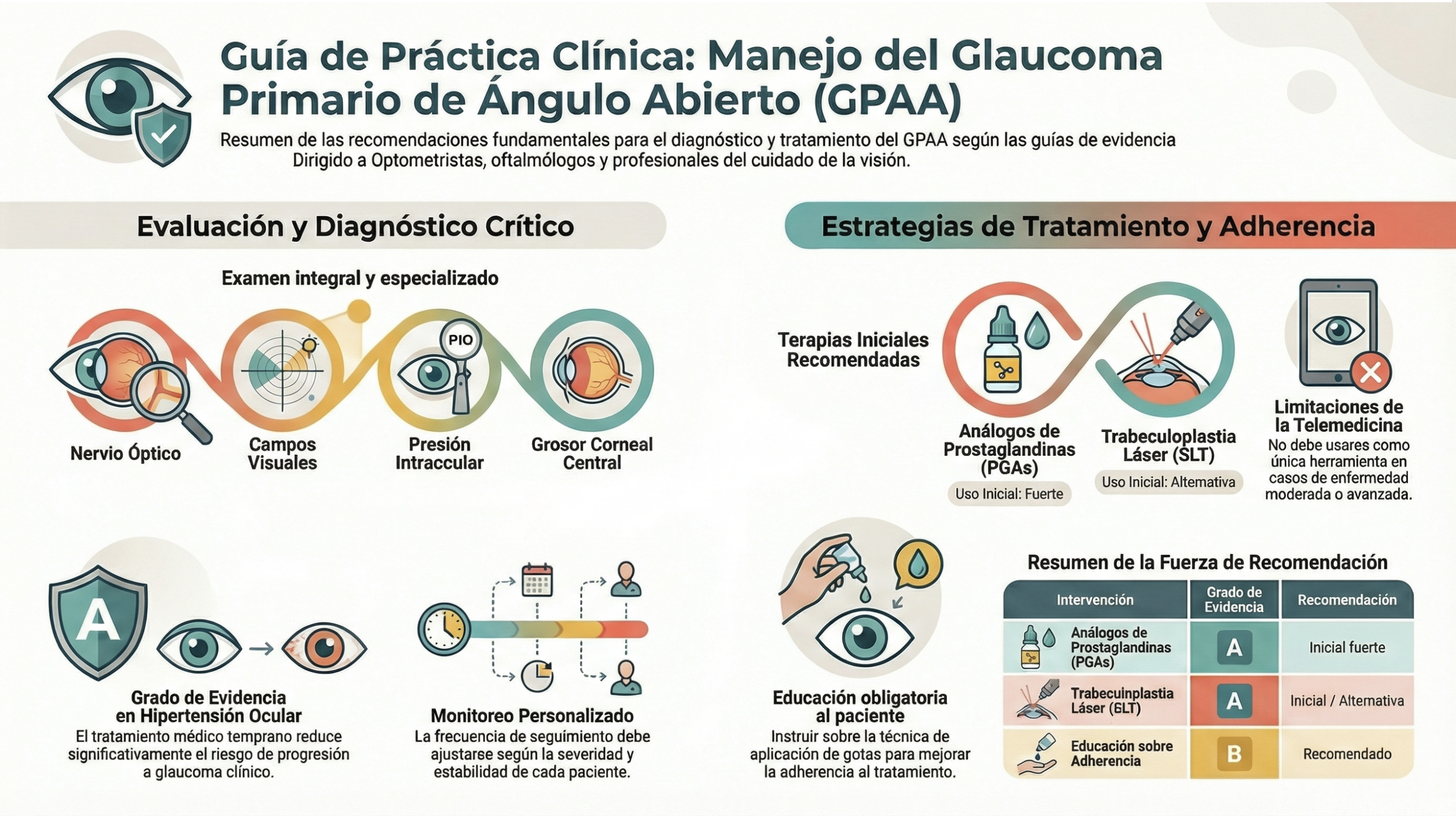
Tratamiento oftalmológico (información para el optometrista)
Conocer las opciones terapéuticas permite al optometrista monitorizar la adherencia, detectar efectos adversos y educar al paciente:
Tratamiento farmacológico (colirios hipotensores)
Trabeculoplastia láser selectiva (SLT)
El ensayo LiGHT (Lancet 2019) demostró que la SLT como tratamiento de primera línea es superior a los colirios en control de PIO a 3 años, con el 74.6% de pacientes libres de colirios tras hasta 2 sesiones de SLT [10]. La SLT se posiciona como alternativa o complemento al tratamiento médico, especialmente para mejorar la adherencia.
El paradigma del “glaucoma intervencionista” está cambiando el enfoque: SLT y MIGS cada vez más precoces, con menor dependencia de colirios crónicos. Profundización en la Guía Avanzada.
Cirugía de glaucoma
- MIGS (cirugía microinvasiva): iStent, Hydrus, canaloplastía, XEN Gel Stent. Menor reducción de PIO que cirugía convencional, pero perfil de seguridad favorable. Frecuentemente combinados con cirugía de catarata [11]
- Trabeculectomía: cirugía filtrante clásica. Reducción potente de PIO pero mayor tasa de complicaciones (ampolla filtrante, hipotónía, endoftalmitis)
- Implantes de drenaje: Ahmed, Baerveldt. Para glaucoma refractario o tras fracaso de trabeculectomía
- Iridotomía láser: tratamiento de primera línea en glaucoma de ángulo cerrado y ángulos ocluibles
Señales de alarma y criterios de derivación
El optometrista es frecuentemente el primer profesional en detectar signos de glaucoma. La derivación oportuna y la comunicación detallada con el oftalmólogo son determinantes para el pronóstico visual.
Derivación urgente (24-48 horas)
- Sospecha de cierre angular agudo: dolor, ojo rojo, PIO muy elevada, edema corneal, pupila mid-midriática arreactiva
- PIO >35 mmHg (riesgo de daño agudo del nervio óptico)
- Pérdida visual aguda o rápida con sospecha de glaucoma
- Glaucoma neovascular (neovasos en iris o ángulo)
- Sospecha de glaucoma congénito: buftalmia, epifora, fotofobia en lactante
Derivación preferente (2-4 semanas)
- Sospecha de glaucoma: excavación aumentada (E/D ≥0.6), asimetría E/D >0.2, pérdida de regla ISNT, hemorragia en astilla
- PIO >24 mmHg confirmada en 2 visitas
- Defecto campimétrico reproducible compatible con glaucoma
- Adelgazamiento de CFNR o CCG en OCT progresivo o significativo
- Ángulo estrecho ocluible (grado 0-1 de Shaffer) sin síntomas agudos
- Progresión documentada en paciente ya diagnosticado a pesar de tratamiento
Derivación a otros profesionales
- Especialista en baja visión: glaucoma avanzado con limitación funcional significativa
- Psicólogo: ansiedad, depresión o dificultad de aceptación del diagnóstico crónico
- Médico de atención primaria: para coordinación de factores sistémicos (HTA, diabetes, apnea del sueño
Herramientas tecnológicas en el manejo del glaucoma
La tecnología ha transformado el diagnóstico y seguimiento del glaucoma. La combinación estructura-función (OCT + campimetría) es el estándar actual para la detección precoz y la monitorización de la progresión.
Profundización en OCT-A en glaucoma, algoritmos de IA para cribado de glaucoma y tonometría domiciliaria en la Guía Avanzada de Tecnología en Optometría.

Consideraciones especiales
Glaucoma y conducción
El glaucoma avanzado con pérdida de campo visual periférico compromete significativamente la seguridad vial. La campimetría estándar (24-2) puede no reflejar adecuadamente el impacto funcional en la conducción. Es necesaria una evaluación del campo visual binocular y de la sensibilidad al contraste en condiciones de baja iluminación.
Adherencia al tratamiento
La adherencia a los colirios hipotensores es uno de los mayores desafíos clínicos: entre el 30-80% de los pacientes no cumplen correctamente el tratamiento. El optometrista debe evaluar activamente la adherencia en cada visita, educar sobre la técnica de instilación, detectar efectos adversos que limiten el cumplimiento y considerar la derivación para SLT o MIGS como alternativa en pacientes con mala adherencia.
Glaucoma normotensivo
Representa el 30-40% de los GPAA. El diagnóstico requiere descartar causas no glaucomatosas de neuropatía óptica (lesión compresiva, isquemia). Los factores vasculares (hipotensión nocturna, vasoespasmo, migraña) son especialmente relevantes. El tratamiento reduce la PIO un 30% respecto a la basal, incluso en rango “normal” [9].
Glaucoma y embarazo
La PIO tiende a disminuir durante el embarazo. La mayoría de los hipotensores oculares están clasificados como categoría C de riesgo teratogénico. En mujeres en edad fértil con glaucoma, es esencial la planificación preconcepcional con el oftalmólogo para ajustar o suspender tratamiento cuando sea posible [12].
Hipertensión ocular
PIO >21 mmHg sin daño del nervio óptico ni defecto campimétrico. No todo paciente con HTO requiere tratamiento. El estudio OHTS demostró que tratar HTO reduce el riesgo de progresión a glaucoma en un 60%, pero la decisión depende de la estratificación de riesgo individual (edad, PIO, ECC, E/D, historia familiar) [5].
Aspectos psicosociales
El diagnóstico de enfermedad crónica irreversible tiene un impacto emocional significativo. La ansiedad relacionada con la posibilidad de ceguera y la carga del tratamiento diario afectan la calidad de vida. El optometrista debe abordar estos aspectos y facilitar apoyo psicológico cuando sea necesario.
Checklist para la práctica clínica
Resumen operativo de acciones clave Optometrista
- Medir PIO con tonometría de aire en todo paciente >40 años (o >35 con factores de riesgo)
- Evaluar el nervio óptico en toda revisión: E/D, asimetría, regla ISNT, hemorragias
- Realizar OCT de CFNR + CCG macular como baseline y para análisis de progresión (si disponemos de OCT)
- Documentar hallazgos con retinografía para seguimiento longitudinal
- Evaluar adherencia al tratamiento y efectos adversos de medicación en cada visita
- Derivar urgente (24-48h) ante sospecha de cierre angular agudo o PIO >35 mmHg
- Derivar preferente ante sospecha de glaucoma, PIO >24 mmHg confirmada o progresión documentada
- Educar al paciente: enfermedad crónica asintomática, importancia de adherencia y revisiones
Resumen operativo de acciones clave Oftalmólogo
- Medir PIO con tonometría de contacto y paquimetría en todo paciente >40 años (o >35 con factores de riesgo)
- Evaluar el nervio óptico en toda revisión: E/D, asimetría, regla ISNT, hemorragias
- Realizar OCT de CFNR + CCG macular como baseline y para análisis de progresión
- Realizar gonioscopía al menos una vez para clasificar el tipo de glaucoma
- Obtener campimetría 24-2 fiable y reproducible (mínimo 2 campos) para confirmar diagnóstico
- Documentar hallazgos con retinografía para seguimiento longitudinal
- Evaluar adherencia al tratamiento y efectos adversos de medicación en cada visita
Este documento es informativo y no sustituye ni a una consulta médica ni optométrica. El diagnóstico definitivo y el plan de tratamiento deben ser efectuados, según el caso, por su oftalmólogo o por su optometrista.
Referencias bibliográficas
- Tham YC, Li X, Wong TY, et al. (2014). Global prevalence of glaucoma and projections of glaucoma burden through 2040. Ophthalmology, 121(11), 2081-2090.
- Stuart KV, de Vries VA, Schuster AK, et al. (2025). Prevalence of glaucoma in Europe and projections to 2050: E3 Consortium. Ophthalmology (in press). DOI: 10.1016/j.ophtha.2025.05.023.
- Anton A, Andrada MT, Mujica V, et al. (2004). Prevalence of primary open-angle glaucoma in a Spanish population: the Segovia study. J Glaucoma, 13(5), 371-376.
- Heijl A, Leske MC, Bengtsson B, et al. (2002). Reduction of intraocular pressure and glaucoma progression: results from the Early Manifest Glaucoma Trial. Arch Ophthalmol, 120(10), 1268-1279.
- Kass MA, Heuer DK, Higginbotham EJ, et al. (2002). The Ocular Hypertension Treatment Study: a randomized trial (OHTS). Arch Ophthalmol, 120(6), 701-713.
- JOGH (2024). Global incidence and risk factors for glaucoma: systematic review and meta-analysis. J Glob Health, 14, 04252.
- European Glaucoma Society. (2021). Terminology and Guidelines for Glaucoma. 5th Edition. Savona: PubliComm.
- Jones R, Rhee DJ. (2006). Corticosteroid-induced ocular hypertension and glaucoma: a brief review. Curr Opin Ophthalmol, 17(2), 163-167.
- Collaborative Normal-Tension Glaucoma Study Group. (1998). Comparison of glaucomatous progression between untreated patients with NTG and patients with therapeutically reduced IOP. Am J Ophthalmol, 126(4), 487-497.
- Gazzard G, Konstantakopoulou E, Garway-Heath D, et al. (2019). Selective laser trabeculoplasty versus eye drops for first-line treatment of ocular hypertension and glaucoma (LiGHT). Lancet, 393(10180), 1505-1516.
- Richter GM, Takusagawa HL, Sit AJ, et al. (2022). Trabecular procedures combined with cataract surgery for open-angle glaucoma: AAO report. Ophthalmology, 129(6), e95-e119.
- Razeghinejad MR, Katz LJ. (2019). Pregnancy and glaucoma. Surv Ophthalmol, 64(5), 580-590.