MINIGUÍA CLÍNICA
Enfermedad del Ojo Seco (EOS)
Ficha rápida
El oftalmólogo es quien diagnostica y trata el ojo seco. El optometrista debe tener conocimientos sobre el ojo seco para derivar los casos sospechosos.
Factores de riesgo
La identificación exhaustiva de los factores de riesgo es esencial, ya que el primer escalón terapéutico del ojo seco es siempre la modificación ambiental y conductual. El TFOS Lifestyle Report (2023) y DEWS III (2025) han reforzado la importancia de los factores de estilo de vida como estrategia transversal de manejo [5, 7].
Factores no modificables
Factores modificables (ambientales, iatrogénicos y de estilo de vida)
El TFOS Lifestyle Report (2023) y DEWS III (2025) han consolidado pantallas, lentes de contacto y cosméticos como factores de riesgo consistentes. Tabaco, cafeína e ingesta de agua no tienen evidencia suficiente aún. Profundización en la Guía Avanzada.
Clasificación clínica
Basada en el consenso TFOS DEWS II/III [1, 5]. La enfermedad del ojo seco es un continuo que casi siempre evoluciona a un cuadro mixto. DEWS III enfatiza que las categorías discretas (leve/moderado/severo; acuodeficiente vs evaporativo) proporcionan una arquitectura subóptima para la toma de decisiones. El enfoque actual identifica los impulsores clínicos relevantes en cada paciente individual [5].
Clasificación por etiología
Estadificación por severidad
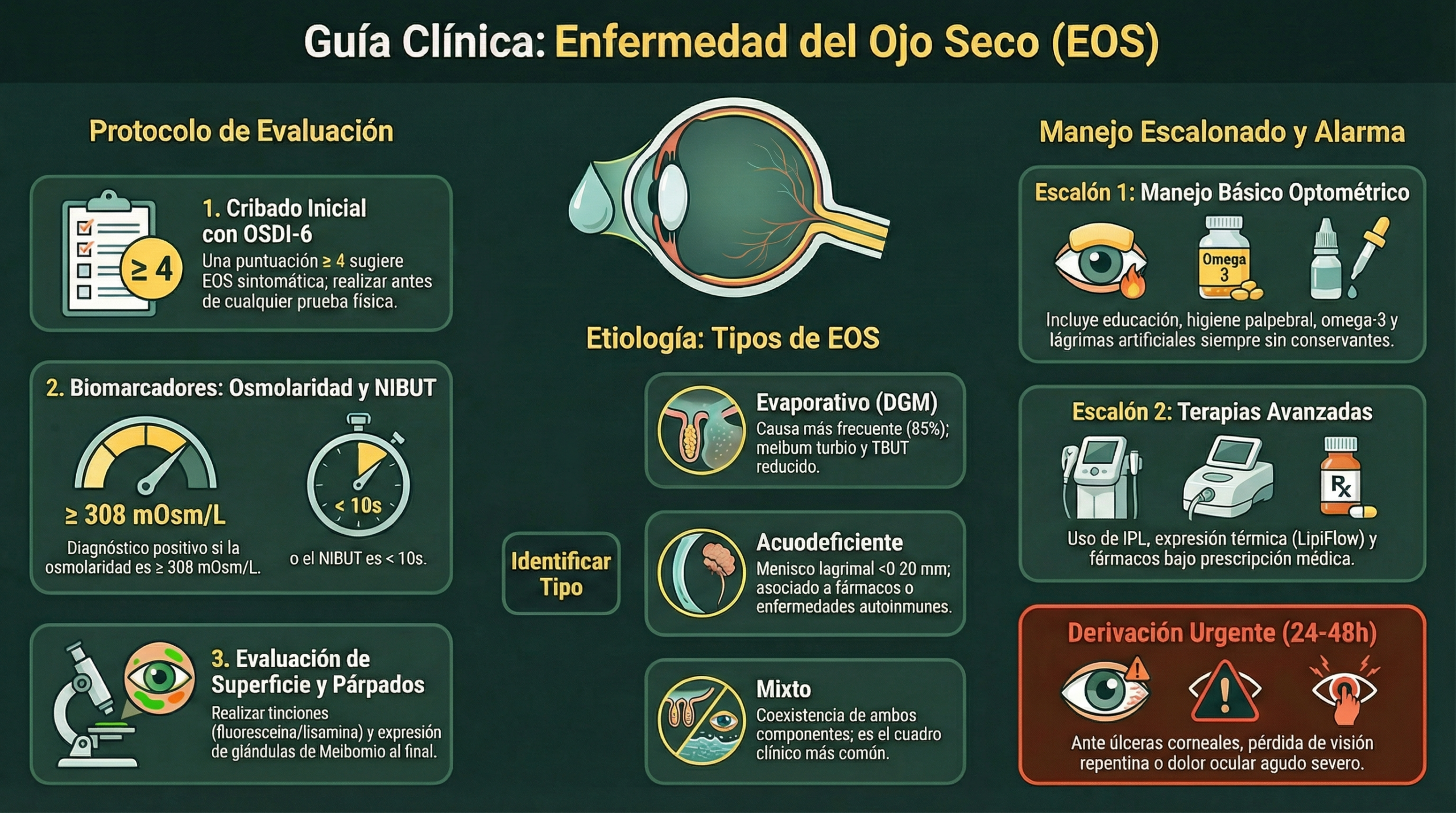
Protocolo de evaluación oftalmológica/optométrica
Los test deben realizarse de menos a más invasivos para no alterar el volumen lagrimal ni inducir hiperemia refleja antes de las mediciones críticas [2, 5].
Anamnesis y cribado
- Cuestionario OSDI-6 (simplificado): Primer paso recomendado por DEWS III. Puntuación ≥4 sugiere EOS sintomática. Sustituye al OSDI-12 como cribado [5]
- Preguntas de exclusión: descartar alergia ocular (picor intenso), infección (secreción mucopurulenta), uveítis, otras patologías de superficie
- Revisión de factores de riesgo/estilo de vida: pantallas, LC, cosméticos, medicación, entorno, cirugía previa [5, 7]
Evaluación instrumental (por orden)
1. Osmolaridad lagrimal (centros muy especializados)
- Marcador central de la enfermedad. Valores ≥308 mOsm/L o asimetría entre ojos >8 mOsm/L son diagnósticos [2, 5]
- Muestra mínima mediante chip lab-on-a-chip (TearLab). Realizar antes de cualquier instilación
2. Menisco lagrimal y NIBUT
- Menisco lagrimal inferior: normal ≥0.20 mm. Valorar con OCT de segmento anterior o topografía
- NIBUT (tiempo de rotura no invasivo): <10 segundos es anormal (criterio DEWS III) [5]. Medición mediante topografía o interferometría, sin instilar fluoresceína
3. Tinción con fluoresceína
- TBUT invasivo: <10 segundos es anormal. Usar volumen mínimo de fluoresceína para no alterar la medición
- Tinción corneal: >5 puntos de tinción con fluoresceína es positivo (criterio DEWS III). Clasificación de Oxford para graduar [5]
4. Tinción con verde lisamina
- Esencial para evaluar: daño en células caliciformes conjuntivales (>9 puntos = positivo, DEWS III), lid wiper epitheliopathy y desplazamiento de la Línea de Marx en el margen palpebral [2, 5]
5. Evaluación de párpados y glándulas de Meibomio
- Presión suave sobre párpado inferior: evaluar calidad (claro, turbio, denso, ausente) y cantidad de expresión del meibum
- Borde palpebral: telangiectasias, irregularidad, queratinización, notching
- Búsqueda de Demodex folliculorum: caspa cilíndrica en base de pestañas (collarettes). Prevalencia alta en >50 años y en blefaritis recurrente [3]
- Parpadeo: evaluar frecuencia y completitud. Parpadeo incompleto es factor de riesgo frecuente
6. Test de Schirmer (si indicado)
- Schirmer I sin anestesia: <10 mm/5 min sospecha de hiposecreción; <5 mm/5 min compatible con déficit acuoso severo
- Realizar al final de la batería de pruebas por su naturaleza invasiva
DEWS III confirma los puntos de corte diagnósticos: NIBUT <10 s, osmolaridad ≥308 mOsm/L, tinción corneal fluoresceína >5 puntos, lisamina conjuntival >9 puntos, lid margin staining ≥2 mm y ≥25% ancho [5]. Estos criterios reemplazan los umbrales menos específicos de DEWS II. Profundización en la Guía Avanzada.
Manejo y seguimiento
Enfoque escalonado basado en TFOS DEWS II/III [3, 5]. DEWS III evoluciona hacia tres algoritmos dirigidos por área (película lagrimal, párpados, superficie ocular), pero el enfoque escalonado sigue siendo operativo para la práctica clínica diaria. Si un escalón no funciona, se pasa al siguiente manteniendo los tratamientos previos que aporten valor.
ESCALÓN 1: Manejo Básico (Optometrista)
- Educación: Explicar la cronicidad de la enfermedad y gestionar expectativas. “No se cura, se controla”
- Estilo de vida: Regla 20-20-20, ejercicios de parpadeo, humidificadores, gafas envolventes. Revisión de cosméticos y LC [7]
- Higiene palpebral: Higiene diaria para DGM, compresas calientes focalizadas (38-42°C, 10 min), limpieza del borde con formulaciones específicas
- Lágrimas artificiales: SIEMPRE sin conservantes. Selección según etiología: base lipídica para DGM, AH/trehalosa para acuodeficiente, combinaciones para mixto
- Nutrición: Suplementación con omega-3 (EPA/DHA alta biodisponibilidad) como “piedra angular” del manejo [3, 5]. Evaluar déficit de B12 y vitamina D
ESCALÓN 2: Manejo Avanzado Clínico (Oftalmología)
- Tratamiento en consulta: Expresión termomecánica de GM (LipiFlow, iLux, MiBo), microblefaroexfoliación (BlephEx), sondaje de glándulas
- IPL (Luz Pulsada Intensa): Para DGM, blefaritis crónica y Demodex. Reduce inflamación, elimina Demodex, estimula función de GM [3]
- Lotilaner 0.25% (Xdemvy): Primer fármaco aprobado específicamente para blefaritis por Demodex (FDA 2023). Ciclo de 6 semanas [5]
- Manejo de la inflamación: Derivación para prescripción de corticosteroides tópicos de baja potencia (loteprednol 0.25% para brotes agudos), ciclosporina tópica (Restasis, Ikervis), lifitegrast (Xiidra) [3, 5]
- Retención lagrimal: Tapones lagrimales de silicona o colágeno (solo si inflamación controlada)
- Perfluorohexiloctano (Miebo): Nueva lágrima semi-fluoro que estabiliza la capa lipídica. Primera aprobación para ojo seco evaporativo (FDA 2023) [5]
ESCALÓN 3/4: Patología Severa y Compleja (Oftalmología y Optometría-Contactología)
- Suero autólogo al 20%: rico en factores de crecimiento y vitamina A. Para queratopatía severa refractaria
- Lentes de contacto esclerales terapéuticas: protegen y nutren la superficie ocular de forma continua (Optometría-Contactología)
- Membrana amniótica: para úlceras tróficas, queratitis neurotrófica, defectos epiteliales persistentes
- Tarsorrafia (parcial o completa): en casos de exposición severa no resoluble
- Neuromodulación: Dispositivos de estimulación nasal (TrueTear/iTear) y neuromoduladores farmacológicos. Área emergente reconocida en DEWS III [5]
- Cirugía de glándula salival: trasplante de glándula submandibular en casos extremos de Sjögren
Señales de alarma y criterios de derivación
La mayoría de los casos de EOS leves se manejan exitosamente en el ámbito optométrico. Sin embargo, determinados hallazgos requieren derivación oportuna.
Derivación urgente (24-48 horas)
- Úlcera corneal o infiltrados corneales (riesgo de perforación o sobreinfección)
- Dolor ocular agudo severo no explicable por los hallazgos superficiales
- Baja visión repentina con fotofobia extrema e hiperemia ciliar (descartar uveítis, queratitis infecciosa)
- Perforación corneal o adelgazamiento corneal severo (descemetocele)
Derivación preferente (2-4 semanas)
- Sospecha de enfermedad autoinmune sistémica (Sjögren): derivar para confirmación serológica
- Queratitis filamentosa severa o placas mucosas adheridas
- Falta de respuesta a escalón 1 de tratamiento tras 2-3 meses
- Necesidad de terapias con prescripción médica (corticoides, ciclosporina, lifitegrast)
- Sospecha de dolor neuropático ocular (síntomas extremos con signos mínimos)
Herramientas tecnológicas en el manejo de la EOS
La evaluación de la superficie ocular ha dejado de ser subjetiva. La incorporación de plataformas analíticas objetivas es fundamental para el diagnóstico preciso, el seguimiento y la educación del paciente. La mayoría de estas tecnologías se pueden encontrar en centros oftalmológicos especializados.
Profundización en plataformas integradas de análisis de superficie ocular (IDRA, Keratograph 5M, Antares), protocolos de IPL y tecnologías emergentes en la Guía Avanzada de Tecnología en Optometría.
Consideraciones especiales
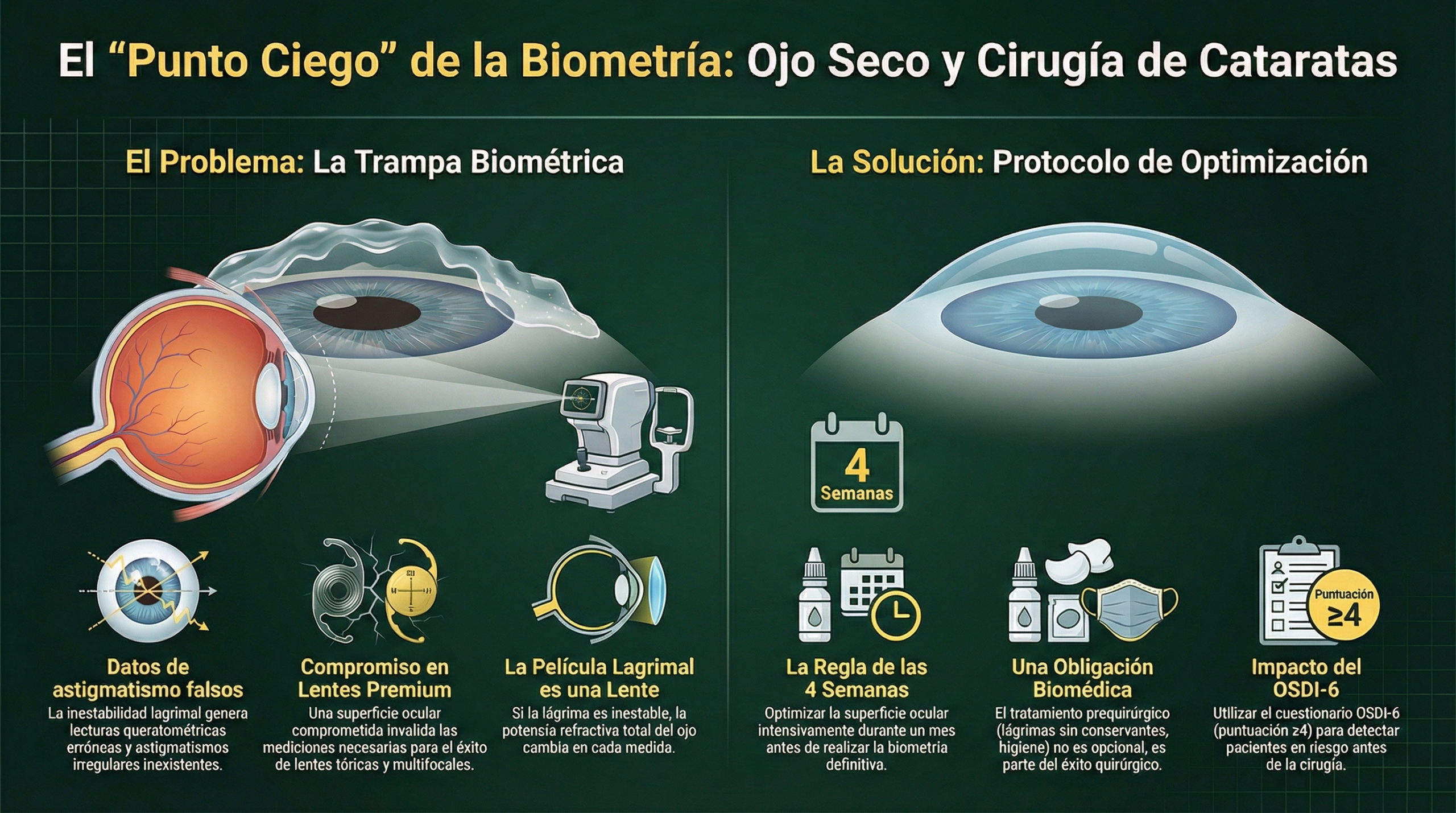
La trampa biométrica prequirúrgica
La película lagrimal es la primera superficie refractiva del ojo. Un paciente con ojo seco no tratado que se somete a biometría para cirugía de cataratas o queratometría para refractiva arrojará datos astigmáticos falsos. Optimizar la superficie ocular durante 4 semanas antes de cualquier medición prequirúrgica es una obligación biomédica, especialmente al implantar lentes premium o tóricas [4].
El dolor neuropático ocular
Cuando los síntomas son extremos, pero la córnea no tiñe y la lágrima es abundante, no se trata de un paciente simulador. Los nervios corneales pueden estar sensibilizados (hiperalgesia) o dispararse espontáneamente. El tratamiento convencional del ojo seco fracasará; requiere un enfoque del dolor crónico mediado por oftalmología y neurología. DEWS III reconoce las anomalías neurosensoriales como uno de los roles etiológicos en la definición actualizada de la enfermedad [5].
EOS y embarazo / lactancia
Los cambios hormonales pueden exacerbar o mejorar la EOS. Muchos fármacos tópicos (ciclosporina, lifitegrast) carecen de datos de seguridad en embarazo. El manejo debe limitarse a lágrimas sin conservantes, higiene palpebral y medidas ambientales. Derivar para cualquier terapia que requiera prescripción.
EOS en jóvenes y pantallas
DEWS III destaca las altas tasas de síntomas en menores de 20 años, impulsadas por el uso de pantallas. La relación entre tiempo de pantalla y EOS es lineal y dosis-dependiente. Los ejercicios de parpadeo consciente y las pausas regulares son la intervención más coste-efectiva en esta población [5, 7].
Omega-3: estado de la evidencia
El estudio DREAM (2018) no encontró beneficio de omega-3 vs placebo en síntomas, pero metaanálisis posteriores muestran evidencia moderada de mejora en signos (Schirmer, TBUT). DEWS III considera la suplementación con omega-3 una “piedra angular” del manejo, aunque reconoce que la evidencia es más sólida para signos que para síntomas [3, 5]. La formulación (EPA/DHA en forma re-esterificada de alta biodisponibilidad) y la dosis importan.
Checklist para la práctica clínica
Resumen operativo de acciones clave:
- Pasar OSDI-6 a todo paciente con quejas de fatiga visual, ardor, sensación de cuerpo extraño o lagrimeo
- Evaluar NIBUT e instilar fluoresceína en lámpara de hendidura en toda revisión ocular
- Realizar presión diagnóstica en párpado inferior para evaluar expresión de meibum en cada paciente
- Prescribir lágrimas según etiología: lipídica para DGM, acuosa para déficit acuoso, combinada para mixto. SIEMPRE sin conservantes
- Buscar Demodex (collaretes en base de pestañas) en toda blefaritis crónica o recurrente
- Educar sobre cronicidad: “No se cura, se controla”. Gestionar expectativas desde la primera visita
- Optimizar superficie ocular 4 semanas antes de CUALQUIER biometría prequirúrgica
- Revisar estilo de vida: pantallas, LC, cosméticos, entorno, nutrición
- Descartar etiología autoinmune en paciente joven con EOS severa + boca seca. Derivar a oftalmología o reumatología
- Derivar urgente ante úlcera corneal, infiltrados o dolor severo inexplicado
Este documento es informativo y no sustituye ni a una consulta médica ni optométrica. El diagnóstico definitivo y el plan de tratamiento deben ser efectuados, según el caso, por su oftalmólogo o por su optometrista.
Referencias bibliográficas
- Craig JP, Nichols KK, Akpek EK, et al. (2017). TFOS DEWS II Definition and Classification Report. Ocul Surf, 15(3), 276-283.
- Wolffsohn JS, Arita R, Chalmers R, et al. (2017). TFOS DEWS II Diagnostic Methodology Report. Ocul Surf, 15(3), 539-574.
- Jones L, Downie LE, Korb D, et al. (2017). TFOS DEWS II Management and Therapy Report. Ocul Surf, 15(3), 575-628.
- Starr CE, Gupta PK, Farid M, et al. (2019). An algorithm for the preoperative diagnosis and treatment of ocular surface disorders. J Cataract Refract Surg, 45(5), 669-684.
- TFOS DEWS III (2025). Diagnostic Methodology, Management and Therapy Reports. Am J Ophthalmol (publicado Q2 2025). Perez VL, Chen W, Craig JP, et al. Executive Summary.
- Benítez-Del-Castillo JM, Burgos-Blasco B (2025). Prevalence of dry eye disease in Spain: PrevEOS study. Ocul Surf, 36, 126-133.
- Craig JP, Alves M, Wolffsohn JS, et al. (2023). TFOS Lifestyle Report Executive Summary: A Lifestyle Epidemic – Ocular Surface Disease. Ocul Surf, 30, 240-253.